
| A. | 硫酸钠晶体俗称芒硝,它是造纸的重要原料 | |
| B. | 澄清的石灰水中滴加碳酸钠溶液有白色沉淀,滴加碳酸氢钠无白色沉淀 | |
| C. | 氟化钠是一种农药,可杀灭地下害虫 | |
| D. | 碳酸氢钠不适合给胃溃疡病人使用 |
分析 A、芒硝是硫酸钠的俗名;
B、碳酸钠、碳酸氢钠都能够与氢氧化钙反应生成沉淀;
C、氟化钠是一种重要的氟盐,主要用作农业杀菌剂、杀虫剂、木材防腐剂和生产含氟牙膏等;
D、小苏打与胃酸中的盐酸反应生成氯化钠、水和二氧化碳气体,患胃溃疡的病人,为防止胃壁穿孔,不能服用小苏打来治疗.
解答 解:A、芒硝是硫酸钠的俗名,所以硫酸钠晶体俗称芒硝,它是造纸的重要原料,故A正确;
B、碳酸钠、碳酸氢钠都能够与氢氧化钙反应生成沉淀碳酸钙,故B错误;
C、氟化钠是一种重要的氟盐,主要用作农业杀菌剂、杀虫剂、木材防腐剂和生产含氟牙膏等,所以氟化钠是一种农药,可杀灭地下害虫,故C正确;
D、小苏打与胃酸中的盐酸反应生成氯化钠、水和二氧化碳气体,患胃溃疡的病人,为防止胃壁穿孔,不能服用小苏打来治疗,故D正确;
故选B.
点评 本题考查钠盐的性质的异同,侧重于学生的分析能力的考查,为高频考点,注意把握Na2CO3和NaHCO3都与氢氧化钙反应生成碳酸钙沉淀,注重基础知识的积累,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 1 mol Na2O2与足量CO2反应后转移的电子数为NA | |
| B. | 1 mol Fe被氧化时,失去的电子数一定为2 NA | |
| C. | 常温常压下,11.2 L CH4中含有的氢原子数为2 NA | |
| D. | 0.1 mol/L MgCl2溶液中Cl-离子数为0.2 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol任何气体的体积都是22.4L | |
| B. | 1mol H2的质量是1g,它所占的体积是22.4L | |
| C. | 在标准状况下,1mol任何气体所占的体积都约为22.4L•mol-1 | |
| D. | 在标准状况下,1mol任何气体所占的体积都约为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3.2mol/L | B. | 1.6mol/L | C. | 0.9mol/L | D. | 无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2可以用来漂白纸浆、毛、丝、草帽辫、增白食品等 | |
| B. | 通信光缆的主要成分是晶体Si,太阳能电池的材料主要是SiO2 | |
| C. | 高锰酸钾溶液、酒精、双氧水都能杀菌消毒,都利用了强氧化性 | |
| D. | 氨很容易液化,液氨气化吸收大量的热,所以液氨常用作致冷剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
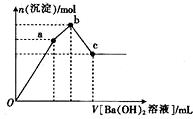 甲是一种可用于净水和膨化食品的盐,由A、B、C、D、E五种短周期元素组成.甲溶于水后可电离出三种离子,其中一种是由A、B形成的10电子阳离子.A元素原子核内质子数比E的少l,D、E同主族.某同学为探究甲的组成而进行如下实验:
甲是一种可用于净水和膨化食品的盐,由A、B、C、D、E五种短周期元素组成.甲溶于水后可电离出三种离子,其中一种是由A、B形成的10电子阳离子.A元素原子核内质子数比E的少l,D、E同主族.某同学为探究甲的组成而进行如下实验:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2Fe3++SO2+2H2O=2Fe2++SO42ˉ+4H+ | B. | Cl2+SO2+2H2O=H2SO4+2HCl | ||
| C. | H2O2+2H++SO42ˉ=SO2↑+O2↑+2H2O | D. | 2Iˉ+2H++H2O2=2H2O+I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 邻二甲苯苯环上的一氯取代产物有4种 | |
| B. | 甲基丙烯酸和甲酸丙酯互为同分异构体 | |
| C. | 乙二醇与甘油互为同系物 | |
| D. | 含5个碳原子的有机物,每个分子中最多可形成5个C-C单键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com