
| A. | 当溶液的pH=7时,溶液的总体积为20mL(若忽略溶液混合后体积的变化) | |
| B. | 在0.1mol/L 的Na2CO3溶液中:c(Na+)+c(H+)═c(CO32-)+c(OH-)+c(HCO3-) | |
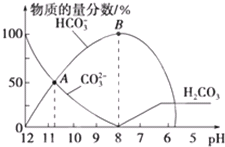
| C. | 在A点所示的溶液中:c(CO32-)═c(HCO3-)>c(H+)>c(OH-) | |
| D. | 在B点所示的溶液中,浓度最大的阳离子是Na+ |
分析 A.当溶液总体积为20mL时,加入的HCl体积是10mL,二者恰好完全反应生成NaHCO3,NaHCO3是强碱弱酸酸式盐,HCO3-水解程度大于其电离程度,溶液呈碱性;
B.任何电解质溶液中都存在电荷守恒,根据电荷守恒判断;
C.根据图知,A点溶液中c(CO32-)═c(HCO3-),溶液的pH>7,溶液呈碱性;
D.B点溶液中溶质为NaHCO3,钠离子不水解,HCO3-水解但程度较小.
解答 解:A.当溶液总体积为20mL时,加入的HCl体积是10mL,二者恰好完全反应生成NaHCO3,NaHCO3是强碱弱酸酸式盐,HCO3-水解程度大于其电离程度,溶液呈碱性,根据图知,pH=7时溶液中的溶质为碳酸氢钠和NaCl,加入的盐酸体积大于10mL,故A错误;
B.任何电解质溶液中都存在电荷守恒,根据电荷守恒得:c(Na+)+c(H+)═2c(CO32-)+c(OH-)+c(HCO3-),故B错误;
C.根据图知,A点溶液中c(CO32-)═c(HCO3-),溶液的pH>7,溶液呈碱性,所以c(H+)<c(OH-),故C错误;
D.B点溶液中溶质为NaHCO3,钠离子不水解,HCO3-水解但程度较小,所以溶液中浓度最大的阳离子是Na+,故D正确;
故选D.
点评 本题考查离子浓度大小比较,为高频考点,侧重考查学生分析判断及识图能力,明确各点溶液中溶质成分及其性质是解本题关键,注意:碳酸钠溶液中滴加稀盐酸时,碳酸钠先生成NaHCO3,然后NaHCO3再和稀盐酸反应,为易错点.


科目:高中化学 来源:2017届江苏省如皋市高三上学期质量调研一化学试卷(解析版) 题型:选择题
硫酸钙可用于生产硫酸、漂白粉等一系列物质(见下图)。下列说法正确的是
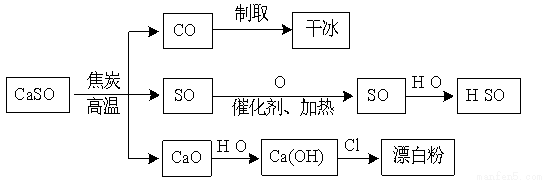
A.CO2制取干冰的过程吸收热量,属于物理变化
B.硫酸钙与焦炭反应时生成的n(CO2):n(SO2)=1:2
C.由SO2制取H2SO4的过程均为氧化还原反应
D.石灰乳与Cl2反应制取漂白粉时,Cl2仅作还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验编号 | HA物质的量浓度(mol/L) | NaOH物质的量浓度(mol/L) | 混合溶液的pH |
| ① | 0.1 | 0.1 | pH=9 |
| ② | c | 0.2 | pH=7 |
| ③ | 0.2 | 0.1 | pH<7 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
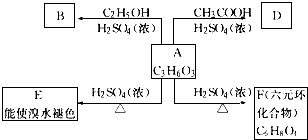
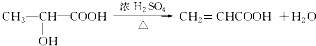 ;A→F
;A→F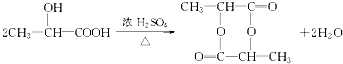
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
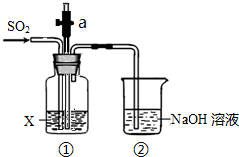 某实验小组用如图所示装置探究SO2的性质.
某实验小组用如图所示装置探究SO2的性质.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
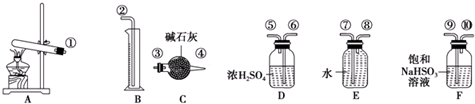
| 实验小组 | 称取CuSO4的质量/g | 装置C增加的质量/g | 量筒中水的体积折算成标准状况下气体的体积/mL |
| 一 | 6.4 | 2.56 | 448 |
| 二 | 6.4 | 2.56 | 224 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
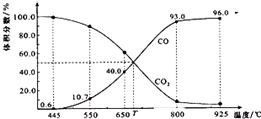 一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g)?2CO(g).平衡时,体系中气体体积分数与温度的关系如图所示:已知:气体分压(p分)=气体总压(p总)×体积分数.下列说法正确的是( )
一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g)?2CO(g).平衡时,体系中气体体积分数与温度的关系如图所示:已知:气体分压(p分)=气体总压(p总)×体积分数.下列说法正确的是( )| A. | 550℃时,若充入惰性气体,v正、v逆 均减小,平衡不移动 | |
| B. | 650℃时,反应达平衡后CO2的转化率为25.0% | |
| C. | T℃时,若充入等体积的CO2和CO,平衡不移动 | |
| D. | 925℃时,用平衡分压代替平衡浓度表示的化学平衡常数Kp=24.p总 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
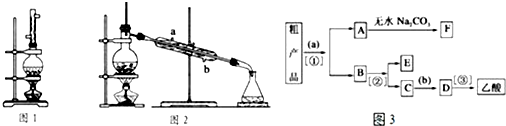
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com