
有机玻璃(聚甲基丙烯酸甲酯)的结构简式可用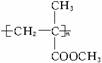 表示。设聚合度n为3 000。
表示。设聚合度n为3 000。
回答下列问题:
(1)指出有机玻璃的单体和链节。
(2)求有机玻璃的相对分子质量。
科目:高中化学 来源: 题型:
Fe2+和Fe3+可以互相转化,现提供的物质有FeCl2溶液、FeCl3溶液、Fe粉、
KSCN溶液、3%H2O2,请你完成实验报告证明Fe2+和Fe3+的互相转化。
| 实 验 步 骤 | 实 验 现 象 | 结 论 |
| 1.①将KSCN溶液滴入盛有FeCl2溶液的试管中,充分振荡 ②再滴入______________,充分振荡 | ①__________________ ②溶液变红 | Fe2+被Cl2氧化成 Fe3+ |
| 2.①在盛有足量Fe粉的试管中滴入FeCl3溶液,充分振荡 ②再滴入KSCN溶液,充分振荡 | ①溶液由___________色变为___________色 ②无明显现象 | __________________________ |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )。
A.冰、水和水蒸气中都存在氢键
B.除稀有气体外的非金属元素都能生成不同价态的含氧酸
C.若ⅡA某元素的原子序数为m,则同周期ⅢA元素的原子序数有可能为m+11
D.干冰升华时分子内共价键会发生断裂
查看答案和解析>>
科目:高中化学 来源: 题型:
下面的表格是元素周期表的一部分,其中的序号对应的是元素。
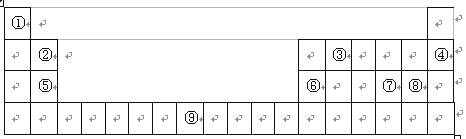
请回答下列问题:
(1) 按原子轨道的重叠方式看,元素①③形成的相对分子质量最小的分子中,含 键;元素⑤和⑧形成的化合键类型为 。
(2) 某元素的价电子排布式为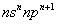 ,该元素与元素①形成的气态化合物分子的空间构型为 。
,该元素与元素①形成的气态化合物分子的空间构型为 。
(3) 表中某元素最外电子层上p电子数比s电子数少1,则该元素的元素符号为
(4) ②④⑤⑥四种元素的第一电离能由大到小的顺序是(填序号) 。
(5) 元素⑨的价电子排布式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
氮的多样性主要体现在含氮化合物及其性质的多样性上,下列说法不正确的是( )
A.用浓硝酸与蛋白质的颜色反应鉴别部分蛋白质
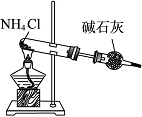
B.实验室可采用如图所示装置制取NH3
C.实验室可用CCl4检验NO2和溴蒸气
D.在常温下,稀硝酸的氧化性强于浓硫酸的
查看答案和解析>>
科目:高中化学 来源: 题型:
不同浓度的硫酸与锌反应时,硫酸可以被还原为SO2,也可被还原为氢气。某校研究性学习小组拟设计实验验证这一事实,并进行数据测定和相关计算。
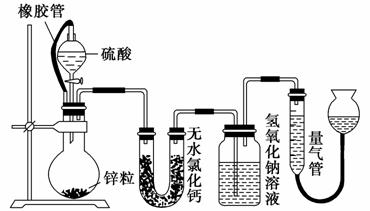
(1)该小组设计了如图所示的实验装置,检查该装置气密性的操作是_______________________________________________________________。
(2)若在烧瓶中放入1.30 g锌粒,与c mol·L-1 H2SO4反应,为保证实验结论可靠,量气管的适宜规格是(填字母)________。
A.100 mL B.200 mL C.400 mL D.500 mL
(3)若1.30 g锌粒完全溶解,氢氧化钠溶液洗气瓶增重0.64 g(烧瓶中残留气体忽略不计,下同),则圆底烧瓶中发生反应的化学方程式为_______________
____________________________________________________________。
(4)若烧瓶中投入a g锌且完全反应,氢氧化钠溶液洗气瓶增重 b g,量气管中收集到V mL气体(标准状况),请用一个代数式表示出a、b、V之间的关系________。
b g,量气管中收集到V mL气体(标准状况),请用一个代数式表示出a、b、V之间的关系________。
(5)若撤走盛有无水氯化钙的U形管,则n(H2)/n(SO2)的数值将________(填“偏大”、“偏小”或“无影响”)。
(6)反应结束后,为了准确测量气体体积,读数时应注意的事项是________、________ 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
锌片与2mol/L H2SO4反应制取氢气时,下列措施能使氢气生成速率加快的是( )
A.向反应体系中加入5mol/L的硝酸溶液提高氢离子浓度
B.将稀H2SO4改用98%浓H2SO4
C. 向反应体系中立即加入大量CuSO4溶液
D. 向反应体系中加入4.5mol/L的盐酸溶液
D. 反应进行80s时,X物质的量浓度为0.04mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com