
有4种碳架如下的烃,下列说法不正确的是
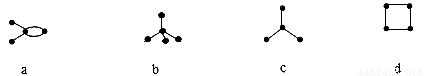
A.a和d是同分异构体 B.b和c是同系物
C.a和d都能发生加成反应 D.只有a能使使酸性KMnO4溶液褪色
科目:高中化学 来源:2017届陕西西安市高三上第二次质量检测化学试卷(解析版) 题型:选择题
O、Si、Al是地壳中含量最多的三种元素,Na、Mg、Cl是海水中的重要元素。下列说法正确的是
A.电解Al2O3和SiO2(少量)的混合物,可以制得较纯净的Al,且有氧气生成
B.从海水中制备Na、Mg、Al、Cl四种元素单质的反应都是氧化还原反应
C.普通玻璃、水泥成分中都含有O、Si、Al三种元素
D.加热蒸干NaCl、MgCl2溶液时可以得到晶体NaCl、MgCl2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省瓦房店市高一上10月月考化学试卷(解析版) 题型:实验题
下图为四种常见的分离提纯方法的装置图。
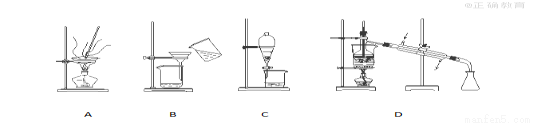
(1)请选择合适的装置分离提纯下列混合物,并用A、B、C、D填空:
① 从食盐水中提取NaCl固体( )
② 分离汽油和水 ( )
( )
③ 分离乙醇(沸点为78℃)和苯酚(沸点为182℃)的混合物( )
④ 除去粗盐溶液中的泥沙( )
(2)B、D装置图中均存在错误,请找出来并用适当的文字表述改进方案:
B:  D:
D:
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省瓦房店市高二上10月月考化学试卷(解析版) 题型:填空题
现有25℃时0.1 mol/L的氨水。请回答以下问题:
(1)若向氨水中加入少量硫酸铵固体,此时溶液中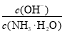 __________(填“增大”“减小”或“不变”)。
__________(填“增大”“减小”或“不变”)。
(2)若向氨水中加入稀硫酸,使其恰好完全中和,写出反应的离子方程式 ;所得溶液的pH_________(填“<”“>”或“=”)7,用离子方程式表示其原因_________________
(3)若向氨水中加入稀硫酸至溶液的pH=7,此时c(NH4+)=a mol·L-1,则c(SO42-)=________。
(4)若向氨水中加入pH=1的硫酸,且氨水与硫酸的体积比为1∶1,则所得溶液中各离子物质的量浓度由大到小的顺序是________ 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省瓦房店市高二上10月月考化学试卷(解析版) 题型:选择题
下列各溶液中,微粒的物质的量浓度关系正确的是
A.10 mL 0.5 mol/L CH3COONa溶液与6 mL 1 mol/L盐酸混合:c(Cl-)>c(Na+)>c(OH -)>c(H+)
-)>c(H+)
B.0.1 mol/L pH为4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-)
C.在NaHA溶液中一定有:c(Na+)+c(H+)=c(HA-)+c(OH-)+c(A2-)
D.c(NH4+)相等的(NH4) 2SO4溶液、(NH4)2CO3溶液和NH4Cl溶液:c[(NH4)2SO4]<c[(NH4)2CO3]<c(NH4Cl)
2SO4溶液、(NH4)2CO3溶液和NH4Cl溶液:c[(NH4)2SO4]<c[(NH4)2CO3]<c(NH4Cl)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省瓦房店市高二上10月月考化学试卷(解析版) 题型:选择题
已知:①2H2(g)+O2(g)=2H2O(l) ΔH=-571. 6kJ·mol-1
6kJ·mol-1
②2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ΔH=-1452kJ· mol-1
mol-1
H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ·mol-1下列说法正确的是
A.H2(g)的燃烧热为571.6kJ·mol-1
B.H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)+2H2O(l)ΔH=-114.6kJ·mol-1
C.同质量的H2(g)和CH3OH(l)完全燃烧,H2(g)放出的热量多
D.3H2(g)+CO2(g)=CH3OH(l)+H2O(l) ΔH=+135.9 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上第二次月考化学试卷(解析版) 题型:填空题
将等物质的量的A、B混合于2  L的密闭容器中,发生如下反应:
L的密闭容器中,发生如下反应:
3A(g)+B(g) xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol/L,
xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol/L,
c(A)∶c(B)=3∶5,C的平均反应速率为0.1 mol/(L·min)。求:
(1)此时A的浓度c(A)=________mol/L,反应开始前容器中的A、B的物质的量:n(A)=n(B)=________mol;
(2)B的平均反应速率v(B)=________mol/(L·min);
(3)x的值为________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省宜春市高二上月考一化学试卷(解析版) 题型:填空题
电离度表示电解质的相对强弱,电离度的定义:
α=(已电离的电解质分子数/溶液中原有电解质的总分子数)×100%。
已知25℃时几种物质(微粒)的电离度(溶液浓度均为0.1 mol·L-1)如下表:
编号 | 物质(微粒) | 电离度α |
A | 硫酸溶液(第一步完 | 10% |
B | 硫酸氢钠溶液:HSO4- | 29% |
C | 醋酸:CH3COOH | 1.33% |
D | 盐酸:HCl=H++Cl- | 100% |
(1)25℃时,0.1 mol·L-1上述几种溶液中,c(H+)从小到大的顺序是 (填序号);
(2)25℃时,0.1 mol·L-1硫酸溶液中HSO4-的电离度小于相同温度下0.1 mol·L-1硫酸氢钠溶液中HSO4-的电离度,其原因是 。
(3)醋酸的电离平衡常数K的表达式是 ,醋酸的电离平衡常数K与电离度α的关系式为:K= (用含α的代数式表示)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林省高二上学期期中化学试卷(解析版) 题型:选择题
反应A(g)+3 B(g)
B(g)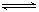 2C(g)+2D(g),在不同情况下测得反应速率,其中反应速率最快的是
2C(g)+2D(g),在不同情况下测得反应速率,其中反应速率最快的是
A.υ(D)=0.4 mol / ?L·s? B.υ(C)=0.5 mol / ?L·s?
C.υ(B)=0.6 mol / ?L·s? D.υ(A)=0.15 mol / ?L·s?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com