
实验题:(共15分)
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯。
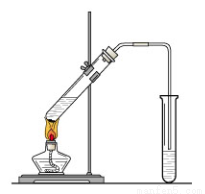
回答下列问题:
(1)写出制取乙酸乙酯的化学反应方程式
(2)在大试管中配制一定比例的乙醇、乙酸和浓硫酸的混合液的方法是 。
(3)浓硫酸的作用是:① ; ② 。
(4)饱和碳酸钠溶液的主要作用是
(5)装置中通蒸气的导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是防止 。
(6)若要把制得的乙酸乙酯分离出来,应采用的实验操作是 。
(7)做此实验时,有时还向盛乙酸和乙醇的试管里加入几块碎瓷片,其目的是 。
(8)生成乙酸乙酯的反应是可逆反应,反应物不能完全变成生成物,反应一段时间后,就达到了该反应的限度,也即达到化学平衡状态。下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有(填序号) 。
①单位时间里,生成1mol乙酸乙酯,同时生成1mol水
②单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
④正反应的速率与逆反应的速率相等
⑤混合物中各物质的浓度不再变化
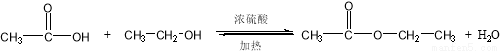
(1)
(2)先在试管中加入一定量的乙醇,然后边加边振荡试管将浓硫酸慢慢加入试管,最后再加入乙酸。
(3)催化作用;吸水作用;(4)中和挥发出来的乙酸,使之转化为乙酸钠溶于水中,便于闻乙酸乙酯的香味,溶解挥发出来的乙醇,降低乙酸乙酯在水中的溶解度,便于分层得到酯。(5)倒吸。(6)分液。(7)防止大试管中液体暴沸而冲出导管。 (8)②④⑤
【解析】
试题分析:(1)乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水,同时该反应可逆,反应的方程式为
(2)在大试管中配制一定比例的乙醇、乙酸和浓硫酸的混合液的方法是先在试管中加入一定量的乙醇,然后边加边振荡试管将浓硫酸慢慢加入试管,最后再加入乙酸。
(3)酸与乙醇需浓硫酸作催化剂,该反应为可逆反应,浓硫酸吸水利于平衡向生成乙酸乙酯方向移动.浓硫酸的作用为催化作用;吸水作用;
(4)制备乙酸乙酯时常用饱和碳酸钠溶液吸收乙酸乙酯,目的是中和挥发出来的乙酸,使之转化为乙酸钠溶于水中,便于闻乙酸乙酯的香味,溶解挥发出来的乙醇,降低乙酸乙酯在水中的溶解度,便于分层得到酯。
(5)a试管受热不均,试管b中的导管伸入液面下可能发生倒吸,导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是防止倒吸.
(6)试管b中的液体不互溶分层,可以分液的方法分离提纯,具体操作为用饱和碳酸钠溶液承接蒸馏出的乙酸乙酯,再分液.
(7)做此实验时,有时还向盛乙酸和乙醇的试管里加入几块碎瓷片,其目的是防止大试管中液体暴沸而冲出导管。
(8)①单位时间里,生成1mol乙酸乙酯,同时生成1mol水,都表示正反应速率,不能说明到达平衡状态,错误;②单位时间里,生成1mol乙酸乙酯表示正反应速率,生成1mol乙酸表示逆反应速率,等于化学计量数之比,说明到达平衡,正确;③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸,都表示正反应速率,不能说明到达平衡状态,错误;④正反应的速率与逆反应的速率相等,说明到达平衡状态,正确;⑤混合物中各物质的浓度不再变化,反应到达平衡状态,正确,选②④⑤。
考点:考查乙酸乙酯的制取,化学平衡状态的判断。


科目:高中化学 来源:2014-2015学年上海市五校高三上学期联合教学质量调研化学试卷(解析版) 题型:选择题
下列反应中,反应后体系中的固态物质增重的是
A.氢气通过灼热的CuO粉末 B.二氧化碳通过Na2O2粉末
C.铝与Fe2O3发生铝热反应 D.将锌粒投入Cu(NO3)2溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015学年陕西省高三上学期12月月考理综化学试卷(A)(解析版) 题型:选择题
海洋中有丰富的食品、矿产、能源、药物和水产资源等(如下图所示),下列有关说法正确的是

A.第①步中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序可以为、NaOH溶液BaCl2溶液,碳酸钠溶液,过滤后加盐酸
B.第②步中结晶出的MgCl2·6H2O可在蒸发皿中加热制无水MgCl2
C.在第④步中的反应离子方程式为Br2+SO2+2H2O=2H+ +SO42-+2HBr
D.第⑤步涉及的分离操作有过滤、萃取、蒸馏
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省高一12月月考化学试卷(解析版) 题型:选择题
下列物质之间的转化都一步能实现的是
A.Si→SiO2→H2SiO3→Na2SiO3 B.Al→Al2O3→Al(OH)3→NaAlO2
C.Na→NaOH→Na2CO3→NaHCO3 D.Cu→CuO→Cu(OH)2→CuSO4
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省高一12月月考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.被氧化的物质是氧化剂
B.可以利用酒精将碘水中的碘提取出来
C.化合反应一定不是氧化还原反应
D.铝抗腐蚀是外层氧化膜致密的缘故
查看答案和解析>>
科目:高中化学 来源:2014-2015陕西省宝鸡市高一上学期期末化学试卷(解析版) 题型:选择题
现有①乙酸乙酯和乙酸钠溶液、②溴化钠溶液和溴水的混合液,分离它们的正确方法依次是
A.分液、蒸馏 B.萃取、分液 C.分液、萃取 D.蒸馏、分液
查看答案和解析>>
科目:高中化学 来源:2014-2015陕西省宝鸡市高一上学期期末化学试卷(解析版) 题型:选择题
市场上有一种加酶洗衣粉,它是在洗衣粉中加入少量的碱与蛋白酶制成的。蛋白酶的催化活性很强,衣物的汗渍、血迹及人体排放的蛋白质、油渍遇到它,都能水解而除去。下列衣料中,不能用加酶洗衣粉洗涤的是
①棉织品 ②毛织品 ③腈纶织品 ④丝织品
A.① B.②③ C.①③ D.②④
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省枣庄市高三1月月考理综化学试卷(解析版) 题型:实验题
(16分)黄铜矿的主要成分是CuFeS2(硫元素显—2价,铁元素显+2价)。实验室里用黄铜矿为原料制取单质铜和铁红(Fe2O3)的流程如下:

已知:CuFeS2+O2 Cu+FeS+ SO2 ,FeS+2HCl
Cu+FeS+ SO2 ,FeS+2HCl FeCl2+H2S。
FeCl2+H2S。
(1)在实验室中,应将黄铜矿粉末放在_____(填仪器名称)中焙烧。
(2)将反应过程中产生的SO2和H2S通入下图所示装置中检验它们的性质。该实验证明SO2具有_________性和__________性。

(3)欲选用下列部分装置在实验室中以MnO2和浓盐酸为原料制取纯净、干燥的氯气。
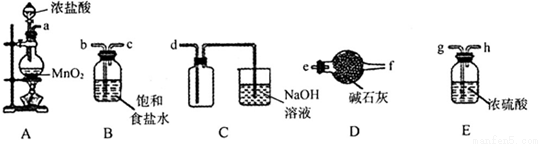
①圆底烧瓶中发生反应的离子方程式为_________________________________________。
②按气流方向由左到右,导管口连接顺序为a→________________________________。
③装置连接好后,需要进行的操作是_________________。
(4)若铁红Fe2O3样品中含有FeO,选用提供的试剂,设计实验验证铁红中含有FeO。写出有关实验操作、现象与结论。________________________________________________________。
提供的试剂:稀盐酸、稀硫酸、KSCN溶液、KMnO4溶液、NaOH溶液、氯水。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年内蒙古巴彦淖尔市高三上学期期中考试化学试卷(解析版) 题型:选择题
下列溶液中,说法正确的是
A.NaHCO3溶液中可以大量存在NO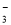 、AlO
、AlO 、K+、S2-等离子
、K+、S2-等离子
B.室温下0.1 mol/L的NaOH溶液与pH=1的某酸HA等体积混合后,溶液中C(Na+)≥C(A-)
C.1 mol/L的醋酸溶液加水稀释时,溶液中所有离子浓度均减小
D.t℃时,水的离子积常数为Kw,则[c(OH-)]2=Kw的水溶液一定呈中性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com