
已知HCl溶液与NaOH溶液的酸碱滴定曲线如下图所示:
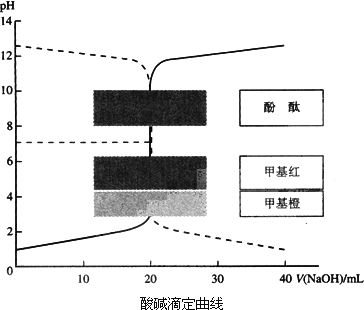
(1)向一定量的NaOH溶液中滴加HCl溶液的曲线为图中________(填“实线”或“虚线”).
(2)下图为对10 mL一定物质的量浓度的硫酸氢钠溶液X用一定物质的量浓度的氢氧化钠溶液Y滴定的图象,依据图象推出X和Y的物质的量浓度分别是________和________.
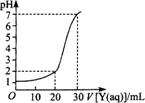
(3)某研究性学习小组的研究课题:食醋中总酸量(g/100 mL)的测定.他们进行以下滴定操作:
A.取某品牌白醋25.00 mL置于________(填仪器名称)中,用蒸馏水稀释10倍.
B.用________(填仪器名称)量取稀释后的白醋溶液20.00 mL,量于250 mL锥形瓶中,滴入________(填指示剂名称)1~2滴.
C.用0.05mol·L-1 NaOH标准溶液滴定,至终点.记下初始与终点读数.(注意:滴定重复进行3次.)
根据以上操作,请你继续回答下列问题.
①(C)中,滴定时,两眼注视________;终点的判断依据是________.
②误差分析:下列操作中能使测定结果偏高的是
a.稀释白醋的蒸馏水预先未经过煮沸处理
b.盛NaOH溶液的碱式滴定管未用标准液润洗
c.滴定前读数正确,滴定终点时俯视读数
d.接近终点时,用少量蒸溜水洗涤锥形瓶.
③如果该小组检测结果与该品牌商标上所注不一致,可能的原因之一是________.
科目:高中化学 来源: 题型:
(16分)炼金废水中含有络离子[Au(CN)2]-,它能电离出有毒的CN-,当CN-与H+结合时生成剧毒的HCN。完成下列问题:
(1)HCN的水溶液酸性很弱,则HCN电离方程式为_________________,NaCN的水溶液呈碱性是因为_________________(用离子方程式表示)。
(2)室温下,如果将0.2mol NaCN和0.1mol HCl全部溶于水,形成混合溶液(假设无损失),①__ _和_ __两种粒子的物质的量之和等于0.2mol。②_ __和_ __两种粒子的物质的量之和比H+多0.1mol。
(3)已知某溶液中只存在OH-、H+、Na+、CN-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:
A、c(CN-)>c(Na+)>c(H+)>c(OH-) B、c(Na+)>c(CN-)>c(OH-)>c(H+)
C、c(CN-)>c(H+)>c(Na+)>c(OH-) D、c(CN-)>c(Na+)>c(OH-)>c(H+)
①若溶液中只溶解了一种溶质,上述离子浓度大小顺序关系中正确的是(填序号) 。
②若上述关系中C是正确的,则溶液中溶质的化学式是_ _和_ 。
③若该溶液中由体积相等的稀HCN溶液和NaOH溶液混合而成,且恰好呈中性,则混合前
c(HCN) c(NaOH)(填“>”、“<”、或“=”下同),
混合后溶液中c(Na+)与c(CN-)的关系c(Na+) c(CN-)。
查看答案和解析>>
科目:高中化学 来源:2013学年海南省琼海市嘉积中学高一下学期教学质量监测(二)理科化学卷(带解析) 题型:填空题
(1)用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4(g)+ 4 NO2 (g)= 4 NO(g)+ CO2 (g)+ 2 H2O(g)ΔH= -574 kJ · mol-1
CH4(g)+ 4 NO(g)= 2 N2(g)+ CO2 (g)+ 2 H2O(g)ΔH= -1160 kJ· mol-1
(1)若用标准状况下4.48L CH4还原NO2至N2,整个过程中转移的电子总数为
(阿伏加德罗常数的值用NA表示),放出的热量为 kJ。
(2)已知稀溶液中,1 mol H2SO4与NaOH溶液恰好完全反应时,放出114.6 kJ热量,写出表示H2SO4与NaOH反应的中和热的热化学方程式_______________________________。
(3)甲硅烷(SiH4)是一种无色液体,遇到空气能发生爆炸性自燃,生成(SiO2)和水。已知室
温下10 g甲硅烷自燃放出热量446 kJ,表示其燃烧热的热化学方程式为:
________________________________________________________________________。
(4)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2是放热反应,当1 mol Cl2参与反应时释放145 kJ的热量,写出这个反应的热化学方程式:
_________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年黑龙江省牡丹江一中高二上学期期中考试化学(理)试卷 题型:填空题
(16分)炼金废水中含有络离子[Au(CN)2]-,它能电离出有毒的CN-,当CN-与H+结合时 生成剧毒的HCN。完成下列问题:
生成剧毒的HCN。完成下列问题:
(1)HCN的水溶液酸性很弱,则HCN电离方程式为_________________,NaCN的水溶液呈碱性是因为_________________(用离子方程式表示)。
(2)室温下,如果将0.2mol NaCN和0.1mol HCl全部溶于水,形成混合溶液(假设无损失),①__ _和_ __两种粒子的物质的量之和等于 0.2mol。②_ __和_ __两种粒子的物质的量
0.2mol。②_ __和_ __两种粒子的物质的量 之和比H+多0.1mol。
之和比H+多0.1mol。
(3)已知某溶液中只存在OH-、H+、Na+、CN-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:
| A.c(CN-)>c(Na+)>c(H+)>c(OH-) | B.c(Na+)>c(CN-)>c(OH-)>c(H+) |
| C.c(CN-)>c(H+)>c(Na+)>c(OH-) | D.c(CN-)>c(Na+)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源:2014届四川省攀枝花市高三第一次统考化学试卷(解析版) 题型:实验题
三氯化磷(PCl3)是一种重要的有机合成催化剂。实验室常用红磷与干燥的Cl2制取PCl3,装置如下图所示。
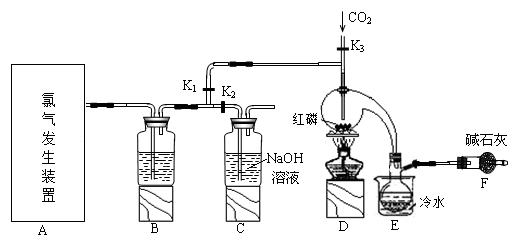
已知:红磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5。PCl3遇O2会生成POCl3(三氯氧磷), POCl3溶于PCl3,PCl3遇水会强烈水解生成H3PO3和HCl。PCl3、POCl3的熔沸点见下表。
|
物质 |
熔点/℃ |
沸点/℃ |
|
PCl3 |
-112 |
75.5 |
|
POCl3 |
2 |
105.3 |
请答下面问题:
(1)B中所装试剂是 ,F中碱石灰的作用是 。
(2)实验时,检查装置气密性后,向D装置的曲颈甑中加入红磷,打开K3通入干燥的CO2,一段时间后,关闭K3,加热曲颈甑至上部有黄色升华物出现时通入氯气,反应立即进行。通干燥CO2的作用是 ,
(3)实验制得的粗产品中常含有POCl3、PCl5等。加入红磷加热除去PCl5后,通过 (填实验操作名称),即可得到较纯净的PCl3。
(4)C装置中的K1、K2的设计也出于类似的目的,为了达到这一实验目的,实验时与K1、K2有关的操作是 。
(5)实验后期关闭K1,打开K2,将气体通入C装置中发生反应,反应后的溶液为X。某同学设计实验来确定溶液X中含有的某些离子,请补充完成实验步骤和现象。
|
实验步骤 |
实验现象 |
实验结论 |
|
① |
|
溶液X中含有Na+ |
|
② |
|
溶液X中含有Cl- |
(5)玻璃管之间的连接需要用到胶皮管,连接的方法是:先把 ,然后稍稍用力即可把玻璃管插入橡皮管。甲同学将装置A的示意图画成右图,该示意图中明显的错误是 。
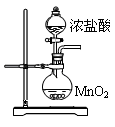
查看答案和解析>>
科目:高中化学 来源:2013学年海南省琼海市高一下学期教学质量监测(二)理科化学卷(解析版) 题型:填空题
(1)用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4(g)+ 4 NO2 (g)= 4 NO(g)+ CO2 (g)+ 2 H2O(g)ΔH= -574 kJ · mol-1
CH4(g)+ 4 NO(g)= 2 N2(g)+ CO2 (g)+ 2 H2O(g)ΔH= -1160 kJ· mol-1
(1)若用标准状况下4.48L CH4还原NO2至N2,整个过程中转移的电子总数为
(阿伏加德罗常数的值用NA表示),放出的热量为 kJ。
(2)已知稀溶液中,1 mol H2SO4与NaOH溶液恰好完全反应时,放出114.6 kJ热量,写出表示H2SO4与NaOH反应的中和热的热化学方程式_______________________________。
(3)甲硅烷(SiH4)是一种无色液体,遇到空气能发生爆炸性自燃,生成(SiO2)和水。已知室
温下10 g甲硅烷自燃放出热量446 kJ,表示其燃烧热的热化学方程式为:
________________________________________________________________________。
(4)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2是放热反应,当1 mol Cl2参与反应时释放145 kJ的热量,写出这个反应的热化学方程式:
_________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com