
下列各溶液中,Na+物质的量浓度最大的是()
A. 2L 0.5mol/L NaCl溶液 B. 3L 0.3mol/L Na2SO4溶液
C. 1L 0.4mol/L Na2CO3溶液 D. 4L 0.15mol/L Na3PO4溶液
考点: 物质的量浓度.
专题: 物质的量浓度和溶解度专题.
分析: 电解质离子的浓度=电解质浓度×电解质电离出该离子的数目,与溶液的体积无关,据此结合选项判断
解答: 解:A、2L 0.5mol/L NaCl溶液中Na+浓度为0.5mol/L×1=0.5mol/L;
B、3L 0.3mol/L Na2SO4溶液Na+浓度为0.3mol/L×2=0.6mol/L;
C、1L 0.4mol/L Na2CO3溶液中Na+浓度为0.4mol/L×2=0.8mol/L;
D、4L0.15mol/L Na3PO4溶液中Na+浓度为0.15mol/L×3=0.45mol/L;
故选C.
点评: 本题考查物质的量浓度,注意电解质溶液中离子的浓度与电解质浓度的计算,题目较简单.


 巧学巧练系列答案
巧学巧练系列答案科目:高中化学 来源: 题型:
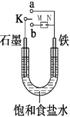
(Ⅰ)如图所示:
(1)若开始时开关K与a连接,则铁发生电化学腐蚀中的________腐蚀。
请写出正极反应式 。
(2)若开始时开关K与b连接时,两极均有气体产生,
则N端是电源的 极(填正或负)则总反应的离子方程式为 。
 |
(Ⅱ)用如图装置电解硫酸钾溶液来制取氧气、氢气、硫酸和氢氧化钾。
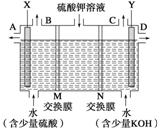
(1)X极与电源的_____(填“正”或“负”)极相连,氢气从_____(填“A、B、C或D”)口导出。
(2)已知离子交换膜只允许一类离子通过,则M为________(填“阴离子”或“阳离子”)交换膜。
(3)若制得标准状况下5.6 L氧气,则生成氢氧化钾的质量是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对物质的量理解正确的是()
A. 物质的量就是物质的质量
B. 物质的量是一种基本物理量
C. 物质的量就是物质的摩尔质量
D. 物质的量就是物质所含粒子的数量
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是()
A. NaCl溶液在电流作用下电离成Na+与Cl﹣
B. 溶于水后能电离出H+的化合物都是酸
C. 液态氯化氢不能导电,但氯化氢是电解质
D. 导电性强的溶液里自由移动离子数目一定比导电性弱的溶液里自由移动离子数目多
查看答案和解析>>
科目:高中化学 来源: 题型:
用CuSO4•5H2O配制500mL、0.1mol•L﹣1CuSO4溶液,完成下列各题
(1)除烧杯、量筒、玻璃棒之外还需要的玻璃仪器有 ;
(2)经计算需要CuSO4•5H2O 克;
(3)有以下操作步骤正确的顺序应为(填序号)
A定容 B溶解 C转移 D注入试剂瓶 E洗涤 F称量
(4)若操作过程中有以下错误,对所配溶液浓度有何影响(填“偏高”、“偏低”或“无影响”)
①进行A操作时俯视刻度线观察
②称量时将砝码和药品的位置放颠倒(1g以下用游码)
(5)取所配溶液10ml,加水稀释到40ml,则稀释后的溶液中溶质的物质的量浓度为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com