
| A. | 60gSiO2晶体中含有2NA个Si-O键 | |
| B. | 18D2O(重水)完全电解,转移2NA个电子 | |
| C. | 1Llmol•L-1 Na2CO3溶液中CO32-数为NA | |
| D. | 16g甲烷含有σ数目为4NA |
分析 A.依据n=$\frac{m}{M}$计算物质的量,结合每个Si原子含有4个Si一0键计算;
B.依据n=$\frac{m}{M}$计算物质的量,结合反应的化学方程式计算电子转移;
C.CO32-为弱酸根,在溶液中会水解;
D.甲烷含有四个C-Hσ键.
解答 解:A.依据n=$\frac{m}{M}$计算物质的量=$\frac{60g}{60g/mol}$=1mol,每个Si原子含有4个Si一0键,60g SiO2晶体中含有4NA个Si一0键,故A错误;
B.依据n=$\frac{m}{M}$计算物质的量=$\frac{18g}{20g/mol}$=0.9mol,结合反应的化学方程式计算电子转移,2D2O$\frac{\underline{\;电解\;}}{\;}$2D2↑+O2↑,0.9mol重水反应电子转移1.8NA,故B错误;
C.CO32-为弱酸根,在溶液中会水解,故溶液中的碳酸根离子的个数小于NA个,故C错误;
D.甲烷分子中含有4个碳氢共用电子对,16个甲烷的物质的量为1mol,含有4mol共用电子对,含有σ数目为4NA,故D正确;
故选:D.
点评 本题考查了阿伏伽德罗常数的判断及计算,熟练掌握物质的量与阿伏伽德罗常数、摩尔质量等物理量之间的关系,注意二氧化硅及甲烷分子的结构,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 反应物是体积比1:3的乙醇和3mol/L硫酸的混和液 | |
| B. | 温度计插入反应溶液液面以下,以便控制反应温度 | |
| C. | 反应容器烧瓶中应加入少许瓷片 | |
| D. | 反应完毕先灭熄灭酒精灯,再从水槽中取出导管 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在酒精灯加热条件下,Na2CO3、NaHCO3固体都能发生分解 | |
| B. | Fe(OH)3胶体无色、透明,能产生丁达尔现象 | |
| C. | H2、SO2、CO2三种气体都可用浓H2SO4干燥 | |
| D. | SiO2既能和NaOH溶液反应又能和氢氟酸反应,所以是两性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 18gD2O和18gH2O中含有的质子数均为10NA | |
| B. | 2L0.5mol/L亚硫酸溶液中含有的H+个数为2NA | |
| C. | 过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA | |
| D. | 密闭容器中2molNO与1molO2充分反应,产物的分子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子中共价键键能越高,键长越长,则分子越稳定 | |
| B. | 元素周期表中的ⅡA族和ⅦA族元素的原子间不能形成共价键 | |
| C. | 水分子可表示为H-O-H,分子中键角为180° | |
| D. | N-N、N=N、N≡N键能之比为1.00:2.17:4.90,说明N2分子中π键键能>σ键键能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 )是无色,带有辛辣气味的易燃液体,有毒.人体吸入过多的苯乙烯蒸气时会引起中毒,在空气中的允许浓度在1×10-4 kg•m-3以下.下列关于苯乙烯的性质推断中正确的是( )
)是无色,带有辛辣气味的易燃液体,有毒.人体吸入过多的苯乙烯蒸气时会引起中毒,在空气中的允许浓度在1×10-4 kg•m-3以下.下列关于苯乙烯的性质推断中正确的是( )| A. | 它能使溴的四氯化碳溶液褪色,但不能使酸性高锰酸钾溶液褪色 | |
| B. | 它既能使溴的四氯化碳溶液褪色,也能使酸性高锰酸钾溶液褪色 | |
| C. | 它易溶于水,也易溶于有机溶剂 | |
| D. | 在一定条件下可以发生加聚反应.生成物可用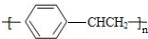 表示 表示 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 7.8g Na2S和Na2O2的混合物中含有的阴离子数等于0.1NA | |
| B. | 12.5mL 16mol•L-1浓硫酸与足量铜反应,转移电子数为0.2NA | |
| C. | 5.6 g铁粉在0.1mol氯气中充分燃烧,转移电子数为0.3NA | |
| D. | 1 mol的甲基与1 mol的铵根离子所含电子数均为10NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com