
| A. | 2个 | B. | 3个 | C. | 4个 | D. | 5个 |
分析 ①根据得失电子判断反应类型;
②原电池的两极不一定是由活动性不同的两种金属组成;
③电解时电解池的阳极可能是金属放电;
④电解稀硫酸制H2、O2时可用铜作阳极,阳极是铜放电得不得氧气;
⑤原电池失去电子的电极称为负极;
⑥阳极是活性金属锌,所以阳极金属锌失去电子发生氧化反应,阴极上溶液中的阳离子即锌离子得到电子变成锌,在铁极上析出;
⑦电解池中,阴离子向阳极移动,阳离子向阴极移动;
解答 解:①电解池阳极上和原电池负极上都是失电子发生氧化反应,故①正确;
②原电池负极上失电子发生氧化反应,电解池阳极上失电子发生氧化反应,故②错误;
③电解时电解池的阳极可能是金属放电,所以电解池的阳极不一定是阴离子放电,故③正确;
④电解稀硫酸制H2、O2时可用铜作阳极,阳极是铜放电得不得氧气,所以用惰性电极,故④错误;
⑤原电池失去电子的电极称为负极,而不是阴极,故⑤错误;
⑥用锌片做阳极,铁片做做阴极,电解氯化锌溶液,这是一个电镀池,镀层金属锌作阳极,待镀件铁作阴极,镀层金属盐氯化锌溶液作电解质,发生反应:阳极:Zn-2e-=Zn2+;阴极:Zn2++2e-=Zn,故⑥正确;
⑦电解池中,阴离子向阳极移动,阳离子向阴极移动,所以用惰性电极电解K2SO4水溶液时,溶液中的SO42-向阳极移动,K+向阴极移动,故⑦正确;
故选C.
点评 本题考查了原电池和电解池原理,难度不大,注意电解时,阳极上不一定是阴离子放电,要根据电极材料判断放电物质或离子.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molO2与金属Na反应,O2一定得到4NA个电子 | |
| B. | 18g NH4+中所含的电子数为11NA | |
| C. | 1molFe与足量的Cl2反应,转移的电子数为2NA | |
| D. | 1molCl2与足量的Fe反应,转移的电子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D | |
| 相 关 实 验 |  | 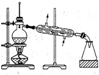 |  | 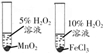 |
| 目的 | 探究接触面积对反应速率的影响 | 分离沸点相差较大的 互溶液体混合物 | 探究温度对化学 平衡的影响 | 探究不同催化剂对反应速率的影响 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将金属钠保存在煤油中 | |
| B. | 少量的白磷可保存在水中 | |
| C. | 纯碱溶液用带磨口玻璃瓶塞的试剂瓶保存 | |
| D. | 硝酸银溶液盛放在棕色试剂瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2与H2O反应:Cl2+H2O═2H++ClO-+Cl- | |
| B. | 向Na2SiO3溶液中逐滴加入稀盐酸:2H++SiO32-═H2SiO3(胶体) | |
| C. | 向AlCl3溶液中滴加氨水至过量:Al3++3OH-═Al(OH)3↓ | |
| D. | 将铜片投入浓硝酸中:2NO3-+3Cu+8H+═3Cu2++2NO2↑+4H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2、O2分别为0.4mol•L-1、0.2mol•L-1 | |
| B. | SO2为0.25mol•L-1 | |
| C. | SO2、SO3均为0.15mol•L-1 | |
| D. | SO3为0.4mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 | |
| B. | 蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 | |
| C. | 分液操作时,上层液体从下口放出 | |
| D. | 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com