
把金属A放入盐B(NO3)2的溶液中,发生如下反应:A+B2+═A2++B,以下叙述正确的是()
A. 常温下金属A一定能与水反应,B一定不能与水反应
B. A与B用导线连接后放入酒精中,一定形成原电池
C. A、B用导线连接后放入B(NO3)2的溶液中,一定有电流产生
D. 由A与B形成的原电池,A一定是正极,B一定是负极
考点: 常见金属的活动性顺序及其应用.
专题: 金属概论与碱元素.
分析: A、在金属活动顺序表中,排在前面的金属可以将后面的金属从其盐中置换出来;
B、根据构成原电池的条件来回答;
C、根据构成原电池的条件来回答;
D、在原电池中,负极金属的活泼性比负正金属的活泼性强.
解答: 解:把金属A放入盐B(NO3)2的溶液中,发生如下反应:A+B2+═A2++B,则失去电子的是金属A,
A、金属Cu放入盐AgNO3的溶液中,发生铜置换银的反应:A+B2+═A2++B,但是金属铜和金属银和水都不反应,故A错误;
B、酒精属于非电解质,A与B用导线连接后放入酒精中,不能形成原电池,故B错误;
C、A、B用导线连接后放入B(NO3)2的溶液中,符合构成原电池的条件,有电流产生,故C正确;
D、由A与B形成的原电 池,失电子的电极A一定是负极,B是正极,故D错误.
池,失电子的电极A一定是负极,B是正极,故D错误.
故选C.
点评: 本题涉及原电池的构成原理以及应用方面的知识,注意知识的梳理和归纳是解题的关键,难度不大.


科目:高中化学 来源: 题型:
下列溶液中Cl﹣的物质的量浓度与100ml 1mol•L﹣1AlCl3溶液中Cl﹣相等的是()
A. 150ml 1 mol•L﹣1氯化钠溶液
B. 75ml 2 mol•L﹣1氯化镁溶液
C. 50ml 3mol•L﹣1氯化钾溶液
D. 200ml 1.5 mol•L﹣1氯化铁溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
某氯化铁样品含有FeCl2杂质.现要测定其中铁元素的质量分数,实验按以下步骤进行:
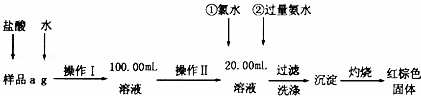
(1)操作I所用到的玻璃仪器除烧杯、玻璃棒外,还必须有 (填仪器名称).
(2)加入过量氨水生成沉淀的离子方程式为
(3)若不用氯水,可用下列试剂中的AC代替(填序号).
A.H2O2 B.碘水 C.NaClO
(4)步骤⑤中检验沉淀是否洗净的方法是 .
(5)若坩埚质量为W1g,坩埚及灼烧后的固体总质量为W2g,样品中铁元素的质量分数为 ×100%(请把结果约到最简).
查看答案和解析>>
科目:高中化学 来源: 题型:
关于氢氧化铁胶体和氯化镁溶液的说法中正确的是()
A. 可用丁达尔现象区分氢氧化铁胶体和氯化镁溶液两种分散系
B. 两者的分散质微粒均能透过半透膜和滤纸
C. 将氢氧化铁固体和氯化镁固体分别溶于水中即可得到氢氧化铁胶体和氯化镁溶液
D. 两种分散系中的分散质微粒直径均介于1~100nm之间
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应既属于氧化还原反应,又是吸热反应的是()
A. 铝片与稀盐酸的反应 B. 灼热的炭与CO2的反应
C. Ba(OH)2•8H2O与NH4Cl的反应 D. 甲烷在氧气中的燃烧反应
查看答案和解析>>
科目:高中化学 来源: 题型:
如图中X、Y分别是直流电源的两极,通电后发现a极板质量增加,b极板处有无色无臭气体放出,如图中符合这一情况的是()
A极板 B极板 X电极 Z溶液
A 锌 石墨 负极 CuSO4
B 石墨 石墨 负极 NaOH
C 银 铁 正极 AgNO3
D 铜 石墨 负极 CuCl2
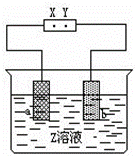
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
LiFePO4电视具有稳定性高、安全、对环境友好等优点,可用于电动汽车.电池反应为:FePO4+Li LiFePO4,电池的正极材料是LiFePO4,负极材料是石墨,电解质为含Li+的导电固体.下列有关LiFePO4电池说法正确的是()
LiFePO4,电池的正极材料是LiFePO4,负极材料是石墨,电解质为含Li+的导电固体.下列有关LiFePO4电池说法正确的是()
A. 可加入硫酸以提高电解质的导电性
B. 放电时电池内部Li+向负极移动
C. 充电过程中,电池正极材料的质量增加
D. 放电时电池正极反应为:FePO4+Li++e﹣=LiFePO4
查看答案和解析>>
科目:高中化学 来源: 题型:
设以为阿伏伽德罗常数的值,下列叙述中正确的是( )
A. 92 g NO2和N204混合气体中含有的原子数为3NA
B. 标准状况下,11.2 L H2O中含有的电子数为20NA
C. 0.5mol•L“的Ba(0H)2溶液中0H一的数目为NA
D. 1 mol Mg与足量的02或N2反应生成MgO或Mg3N2时,失去的电子数均为2N
查看答案和解析>>
科目:高中化学 来源: 题型:
反应4NH3(g)+5O2(g)⇌4NO(g)+6H2O(g),在10L的密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率V(x)可表示为()
A. V(NH3)=0.0010mol•L﹣1•S﹣1 B. V(O2)=0.0010 mol•L﹣1•S﹣1
C. V(NO)=0.010 mol•L﹣1•S﹣1 D. V(H2O)=0.045 mol•L﹣1•S﹣1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com