
| 反应时间/min | n(CO2)/mol | H2/mol |
| 0 | 1.50 | 1.00 |
| t1 | 0.40 | |
| t2 | 0.90 |
A、反应在t1min内的平均速率为v(H2O)=
| ||
| B、温度升至800℃,上述反应平衡常数为1.56,则正反应为放热反应 | ||
| C、保持其他条件不变,向平衡体系中再通入1.00mol H2,与原平衡相比,达到新平衡时CO2转化率增大,H2的体积分数增大 | ||
| D、保持其他条件不变,起始时向容器中充入1.00mol CO和1.50mol H2O,到达平衡时,c(CO2)=0.90mol/L |
| ||
| t1min |
| 0.6 |
| t1 |
| 0.6 |
| t1 |
| 0.6×0.6 |
| 0.9×0.4 |
| 0.6×0.1 |
| 0.9×0.9 |


 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案 新思维寒假作业系列答案
新思维寒假作业系列答案科目:高中化学 来源: 题型:

| 催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 此图装置探究NaHCO3的热稳定性 |
B、 此图装置Cl2的收集 |
C、 此图装置向容量瓶中转移液体 |
D、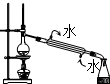 此图装置石油蒸馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、工业电解饱和食盐水:2Cl-+H2O=Cl2↑+H2↑+OH- | ||
| B、碳酸钠的水解:CO32-+2H2O?H2CO3+2OH- | ||
C、硫酸铝溶液中滴加过量浓氨水:Al3++4OH-═AlO
| ||
| D、用过氧化氢从酸化海带灰浸出液中提取碘:2I-+H2O2+2H+=I2+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、用Pt电极电解少量的CuCl2溶液:2H2O+Cu2++2Cl-
| ||||
| B、0.01mol/L NH4Al(SO4)2溶液与0.02mol/L Ba(OH)2溶液等体积混合NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3?H2O | ||||
| C、酸性高锰酸钾溶液中滴加H2O2溶液:4H2O2+4MnO4-+12H+=4Mn2++10H2O+7O2↑ | ||||
| D、向磁性氧化铁中加入氢碘酸:Fe3O4+8H+=Fe2++2Fe3++4H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ca(ClO)2溶液中通入过量的CO2:Ca2++2ClO-+CO2+H2O=CaCO3↓+2HClO |
| B、钠和冷水反应:Na+2H2O=Na++2OH-+H2↑ |
| C、氯气和水反应:Cl2+H2O=2H++Cl-+ClO- |
| D、FeCl2溶液中滴加氯水:2Fe2++Cl2=2Fe3++2Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、增大A浓度的瞬间,V正增大,V逆不变 |
| B、升高温度,V正减小,V逆增大 |
| C、增大压强.V正增大,V逆减小 |
| D、加入催化剂,V正、V逆都增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.250 | 0.012 |
| 容器 | 甲 | 乙 | 丙 | |
| 反应物投入量 | 1molCO 2molH2 | 1molCH3OH | 2molCH3OH | |
| 平衡数据 | CH3OH的浓度(mol/L) | c1 | c2 | c3 |
| 反应的能量变化的绝对值(kJ) | a | b | c | |
| 体系压强(Pa) | P1 | P2 | P3 | |
| 反应物转化率 | α1 | α2 | α3 | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com