

| A、X元素的化合价可能为+4价 |
| B、X为非金属 |
| C、X为第五周期元素 |
| D、X与氯气反应最可能生成的化合物的化学式可能为XCl3 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
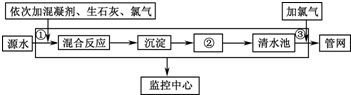 如图是目前我国城市饮用水的生产流程,生活饮用水水质的标准主要有:色度、浑浊度、pH、细菌总数、气味等.
如图是目前我国城市饮用水的生产流程,生活饮用水水质的标准主要有:色度、浑浊度、pH、细菌总数、气味等.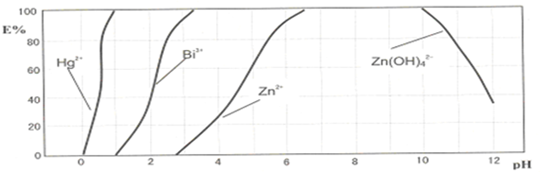
查看答案和解析>>
科目:高中化学 来源: 题型:
 研究确定六氟化硫分子为正八面体构型(分子结构如图所示),难溶于水,在高温下仍有良好的绝缘性,在电器工业方面具有广泛用途.下列推测正确的是( )
研究确定六氟化硫分子为正八面体构型(分子结构如图所示),难溶于水,在高温下仍有良好的绝缘性,在电器工业方面具有广泛用途.下列推测正确的是( )| A、SF6中各原子均达到8电子稳定结构 |
| B、SF6分子中既含有非极性共价键键又含有极性共价键 |
| C、SF6分子是含有极性键的非极性分子 |
| D、SF6可能是原子晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、晶体硅熔点高硬度大,可用于制作半导体材料 |
| B、浓硫酸具有酸性,可用于刻蚀玻璃制品 |
| C、漂白粉在空气中不稳定,可用于漂白纸张 |
| D、氢氧化铝具有弱碱性,可用于制胃酸中和剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③ | B、②③ |
| C、③④ | D、③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、稀硫酸跟铁反应:Fe+6H+=2Fe3++3H2↑ |
| B、稀硫酸与氢氧化钡溶液反应:H++OH-=H2O |
| C、碳酸钙放入稀盐酸中:CO32+2H+=CO2↑+H2O |
| D、稀盐酸放入碳酸钠中:CO32+2H+=CO2↑+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com