
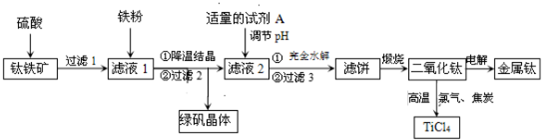
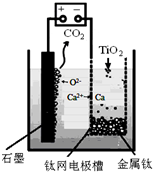
分析 钛铁矿用硫酸溶液溶解,过滤得强酸性溶液中含有TiOSO4、FeSO4及未反应的硫酸等,由图1可知TiO(OH)2与Fe(OH)3沉淀的pH很接近,所以加入铁粉目的是将Fe3+转化为Fe2+,防止Fe3+与TiO2+同时生成沉淀,沉降分离得到溶液中主要含有Fe2+、TiO2+及硫酸根,再浓缩蒸发得到绿矾与溶液Ⅱ,溶液Ⅱ中含有TiOSO4,加入碳酸镁,调节pH,TiO(OH)2沉淀完全,再经过系列操作得到Ti.
(1)钛铁矿主要成分FeTiO3与浓硫酸反应的主要产物是TiOSO4和FeSO4,结合原子守恒配平书写化学方程式;
(2)滤液1中加入适量铁粉至浸出液显紫色,说明浸出液中含有Ti3+;
(3)加入MgCO3粉末与H+反应,降低了溶液中c(H+),使平衡TiO2++(n+1)H2O?TiO2•n H2O+2H+向生成TiO2•n H2O的方向移动,可得到TiO2粗产品;
(4)根据盖斯定律进行计算;
(5)电解时,阴极发生还原反应生成Ti;
(6)根据FeTiO3中铁与钛的关系及铁元素的守恒可计算.
解答 解:钛铁矿(主要成分FeTiO3,含Fe2O3、SiO2等杂质)加入浓硫酸加热反应得到固体熔块,加入水水浸,得到浸取液中加入铁屑防止亚铁离子被氧化为铁离子,过滤得到X晶体为为绿矾(FeSO4•7H2O)晶体和滤液TiOSO4,加入水反应生成H2TiO3,高温煅烧得到二氧化钛,
(1)钛铁矿主要成分FeTiO3与浓硫酸反应的主要产物是TiOSO4和FeSO4,结合原子守恒配平书写化学方程式为:FeTiO3+2H2SO4═FeSO4+TiOSO4+2H2O,故答案为:FeTiO3+2H2SO4═FeSO4+TiOSO4+2H2O;
(2)加入铁屑至浸出液显紫色,说明浸出液中含有Ti3+,加入铁屑作还原剂,将Fe3+还原为Fe2+,防止Ti3+被Fe3+氧化成TiO2+,故答案为:使Fe3+完全还原为Fe2+;同时避免过量的铁将TiO2+还原成Ti3+,影响产品的纯度;
(3)富含的TiO2+溶液,加入MgCO3粉末与H+反应,降低了溶液中c(H+),使平衡TiO2++(n+1)H2O?TiO2•n H2O+2H+向生成TiO2•n H2O的方向移动,可得到TiO2粗产品,故答案为:b;
(4)由△H3+△H1×2-△H2得:+141kJ•mol-1+(-393.5kJ•mol-1)×2-(-566kJ•mol-1)=-80KJ/mol,故答案为:-80KJ/mol;
(5)电解时,阴极发生还原反应生成Ti,电极方程式为TiO2+4e-=Ti+2O2-,故答案为:TiO2+4e-=Ti+2O2-;
(6)由FeTiO3中铁与钛的关系的钛的含量为:$\frac{48}{56}×a%$.
设铁元素总质量为xkg.
Fe~FeSO4•7H2O
56 278
xkg×80% ckg
x=$\frac{56c}{278×80%}$kg.
FeTiO3中铁的质量为:($\frac{56c}{278×80%}$kg-bkg)×a%.
又设得到TiO2质量为为ykg.
Ti~TiO2
48 80
($\frac{56c}{278×80%}$kg-bkg)×a%×$\frac{48}{56}$×90% y
y=(3.247ac-12.86ab)×10-3 kg
故答案为:(3.247ac-12.86ab)×10-3.
点评 本题考查了硫酸法制取二氧化钛实验,涉及物质提纯、分离、制备等流程分析判断,把握物质的性质、反应原理、实验技能、关系式计算为解答的关键,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 称量后转移固体时不小心把少量固体洒到烧杯外 | |
| B. | 加水定容时,加水过多,倒出后并恢复到刻度线水平 | |
| C. | 转移过程中不小心把几滴溶液滴在外面 | |
| D. | 干净的容量瓶又用蒸馏水洗涤了一遍 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝是还原剂,其氧化产物是H2 | B. | NaOH是氧化剂,其还原产物是H2 | ||
| C. | 铝是还原剂,H2O和NaOH都是氧化剂 | D. | H2O是氧化剂,Al被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
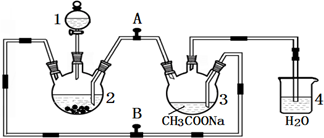 醋酸亚铬水合物
醋酸亚铬水合物查看答案和解析>>
科目:高中化学 来源: 题型:解答题
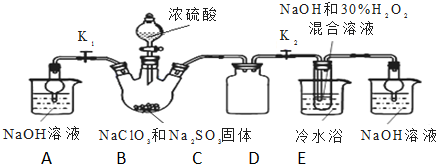
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
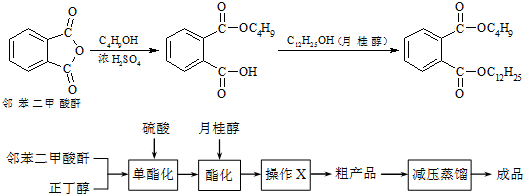
| 化合物 | 溶解性 | 熔点 | 沸点 |
| 邻苯二甲酸酐 | 微溶于冷水、乙醚,易溶于热苯、乙醇、乙酸 | 131.6℃ | 295℃ |
| 正丁醇 | 微溶于水,溶于乙醇、醚、多数有机溶剂 | -88.9℃ | 117.5℃ |
| 月桂醇 | 不溶于水,溶于醇、醚 | 24 | 259℃ |
| 邻苯二甲酸丁基月桂酯 | 不溶于水,溶于多数有机溶剂 | 不祥 | 202~210℃ |
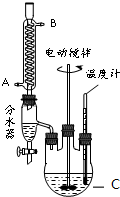
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
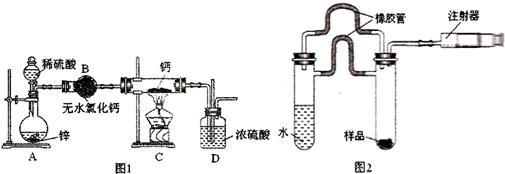
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化石能源物质内部蕴涵着大量的能量 | |
| B. | 绿色植物进行光合作用时,将太阳能转化为化学能“贮存”起来 | |
| C. | 吸热反应中由于反应物总能量小于生成物总能量,因而没有利用价值 | |
| D. | 物质的化学能可以在一定条件下转化为热能.电能为人类所利用 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
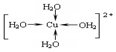 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com