
【题目】在恒容条件下,反应:2SO2 (g) + O2 (g) ![]() 2SO3(g) ΔH =-QkJ·mol-1。在上述条件下分别充入的气体和反应放出的热量 ( Q>0 )如下表所列:
2SO3(g) ΔH =-QkJ·mol-1。在上述条件下分别充入的气体和反应放出的热量 ( Q>0 )如下表所列:
容器 | SO2 (mol) | O2(mol) | N2(mol) | Q(kJ·mol-1) |
甲 | 2 | 1 | 0 | Q1 |
乙 | 1 | 0.5 | 0 | Q2 |
丙 | 1 | 0.5 | 1 | Q3 |
根据以上数据,下列叙述正确的是( )
A. 在上述条件下反应生成lmol SO3固体放热Q/2 kJ B. 2Q3 <2Q2=Q1<Q
C. Ql =2Q2= 2Q3 = Q D. 2Q2 = 2Q3 < Q1 < Q
【答案】D
【解析】A.2SO2(g)+O2(g)2SO3(g)△H=-QkJ/mol,在上述条件下反应生成1molSO3气体放热0.5QkJ,生成1molSO3固体放出的热量大于0.5QkJ,A错误;B.乙、丙两个容器容积相同,所充气体物质的量相同,丙中所充氮气对平衡无影响,所以乙、丙建立等效平衡,二氧化硫转化率相同,Q2=Q3;甲、乙两个容器容积相同,甲中相应物质的物质的量为乙中2倍,压强比乙中高,相对乙平衡而言甲中平衡右移,二氧化硫转化率增大,所以甲中放出的热量大于乙甲中的2倍,可逆反应不能完全反应,故2Q2<Q1<Q,综上所述所述,2Q2=2Q3<Q1<Q,B错误;C.由B中分析可知,2Q2=2Q3<Q1<Q,C错误;
D.由B中分析可知,2Q2=2Q3<Q1<Q,D正确;答案选D。


 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】向100mL碘化亚铁溶液中缓慢通入标况下4.48L氯气,完全反应后,溶液中有一半的Fe2+未被氧化,则原碘化亚铁溶液的物质的量浓度是( )
A. 1.2mol/L B. 1.5mol/L C. 1.6mol/L D. 2.0mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】作为高中生,学会利用我们课堂上学到的知识来解决生活中的一些问题,是我们学习的重要目的之一.成外某化学实验兴趣小组,一行四人,利用实验室老师提供的基本仪器和药品,自行购置了鸡蛋,食醋等生活用品,进行了如下探究.
I.甲同学老家在阆中,对儿时在家乡品尝到的阆中老陈醋的滋味记忆犹新,跟随父母来到成都后,总是觉得超市买到的醋不如儿时的味道,查阅相关资料后,得知如图1信息:
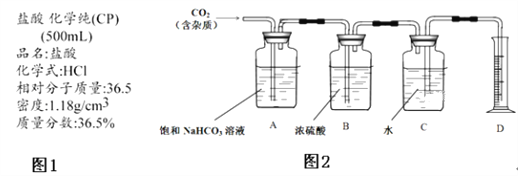
①醋分两种,酿造醋和配制醋.正宗的老陈醋必须经长久时间酿造才得此美味,市场上多充斥着工业醋酸加水勾兑的配制醋.
②酿造醋国家标准为醋酸含量必须大于3.50g/100mL,而配制醋国家标准仅为1.50g~3.50g/100mL.
③在老师的帮助下,测定了超市购买的食醋中,醋酸的物质的量浓度为0.75mol/L.
(1)请帮助甲同学计算从超市购买的食醋中醋酸含量为_____g/100mL,属于_____醋(填“酿造”或“配制”).(提示:醋酸摩尔质量为60g/mol)
(2)请写出醋酸与鸡蛋壳(主要成分为CaCO3)反应的离子方程式_____。
II.如图1是成外化学实验室浓盐酸试剂标签上的部分内容.乙同学现用该浓盐酸配制100mL 1molL﹣1的稀盐酸.可供选用的仪器有:①胶头滴管;②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平;⑦玻璃棒.请回答下列问题:
(1)配制稀盐酸时,还缺少的仪器有_____;
(2)经计算,配制100mL1molL﹣1的稀盐酸需要用量筒量取上述浓盐酸的体积为_____mL(保留小数点后一位);
(3)对所配制的稀盐酸进行测定,发现其浓度小于1molL﹣1,引起误差的原因可能是_____。
A.定容时俯视容量瓶刻度线
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.转移溶液后,未洗涤烧杯和玻璃棒
D.定容摇匀后发现液面低于容量瓶的刻度线,再加水至刻度线
III.丙同学对课堂上学到的胶体的相关知识产生了浓厚兴趣.
(1)他利用买来的鸡蛋的蛋清配制成溶液,用激光笔照射溶液,发现一条光束穿过鸡蛋清溶液,此现象称为_____。
(2)他将乙同学配制好的盐酸溶液加入到鸡蛋清溶液中,发现出现絮状沉淀,此现象称为_____。
IV.丁同学试图测定CO2的相对分子质量.
①利用丙同学用完后剩下的鸡蛋壳和乙同学配制好的稀盐酸溶液制备CO2;
②查询相关书籍后,设计了如图2所示装置:
(1)其他同学认为B装置在此处没必要,请简述原因_____。
(2)A装置中的饱和NaHCO3溶液可以吸收_____。
(3)实验前测得C装置(含水)重量为50.00g,实验完毕后C装置(含水)重量为40.02g,D中量筒读数为10.0mL,已知H2密度为0.09g/L(以上数据均已折合为标况下数值),请根据以上数据,计算CO2的相对分子质量为_____(保留小数点后一位).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。下列分析正确的是( )
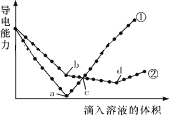
A.②代表滴加H2SO4溶液的变化曲线
B.b点溶液中大量存在的离子是SO42-、Na+、OH-
C.a、d两点对应的溶液均显中性
D.c点两溶液中含有相同量的OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,电解质溶液中的下列关系式不正确的是( )
A. 已知A-+H2B(过量)![]() HA+HB-,则结合H+的能力:HB-<A-<B2-
HA+HB-,则结合H+的能力:HB-<A-<B2-
B. 在0.1 molL-1的氨水中滴加0.1 molL-1盐酸,恰好完全中和时溶液的pH=a,则由水电离产生的c(OH-)=10-a molL-1
C. 将c molL-1的醋酸溶液与0.02 molL-1NaOH溶液等体积混合后溶液恰好呈中性,用含c的代数式表示CH3COOH的电离常数Ka=![]()
D. 将0.2 mol·L-1盐酸与0.1 mol·L-1的KAlO2溶液等体积混合,溶液中离子浓度由大到小的顺序:c(Cl-)>c(K+)>c(Al3+)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】250℃时,14gCO2和H2O(g)的混合气体与足量的Na2O2反应,反应后固体质量增加了6g,则原混合物的平均相对分子质量为
A. 36 B. 22 C. 28 D. 42
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为V L的某密闭容器中,a mol CO与2a mol H2在催化剂作用下反应生成甲醇:CO(g)+2H2(g)![]() CH3OH(g)。CO的转化率与温度、压强的关系如图所示:
CH3OH(g)。CO的转化率与温度、压强的关系如图所示:
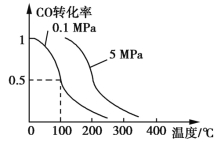
(1)该反应是 反应(填“放热”或“吸热”)。
(2)在压强为0.1 MPa条件下,200 ℃时,该反应的平衡常数K (填“=”“<”或“>”)V2/a2。
(3)在温度、容积不变的情况下,向该密闭容器再增加a mol CO(g)、2a mol H2(g)和b mol CH3OH(g),则达到新平衡时,CO的转化率 (填“增大”“减小”“不变”或“无法确定”),平衡常数 (填“增大”“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解硫酸钠溶液生产硫酸和烧碱溶液的装置如图所示,其中阴极和阳极均为惰性电极。测得同温同压下,气体甲与气体乙的体积比约为1∶2,以下说法正确的是( )

A. a极与电源的负极相连
B. a电极反应式:2H2O+2e-= H2↑+2OH-
C. 离子交换膜d为阴离子交换膜
D. 产物丙为硫酸溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com