


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
| A、①③④ | B、①②③ |
| C、③⑥ | D、①②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、漂白粉的有效成分是Ca(ClO)2 |
| B、铁锈的主要成份是四氧化三铁 |
| C、NO、NO2是大气污染物,能在空气中稳定存在 |
| D、HNO3和H2SO4都是很难挥发的酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(OH-)=c(HS-)+c(H+)+c(H2S) |
| B、c(OH-)=c(HS-)+c(H+)+2 c(H2S) |
| C、c(Na+)=c(S2-)+c(HS-)+c(H2S) |
| D、c(Na+)+c (H+)=c(HS-)+c(OH-)+c(S2-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下,pH=2的H2SO4溶液中含有的H+离子数目为0.01NA |
| B、常温常压下,3.2 g CH4中含有电子2NA |
| C、标准状况下,11.2 L CH3CH2OH中含有分子0.5NA |
| D、100 mL 1 mol?L-1的CH3COOH溶液中含有CH3COOH分子0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铁片上镀锌的阴极 |
| B、电解氯化铜溶液时的阴极 |
| C、电解食盐水时的阴极 |
| D、铜锌原电池的负极(硫酸溶液为电解质) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入适量的6 mol/L的盐酸 |
| B、加入数滴硝酸铜溶液 |
| C、加入适量蒸馏水 |
| D、无答案 |
查看答案和解析>>
科目:高中化学 来源: 题型:
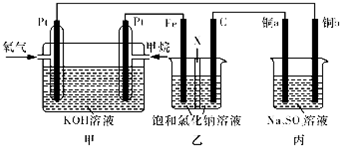
查看答案和解析>>
科目:高中化学 来源: 题型:
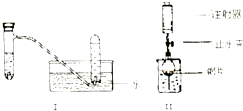 如图是铜与稀硝酸反应的两个实验装置图,谘冋答下列问题:
如图是铜与稀硝酸反应的两个实验装置图,谘冋答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com