
分析 (1)4FeS2+11O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+8SO2,根据硫元素守恒,得到关系式:FeS2~2SO2~2SO2~2H2SO4,取该硫酸2.45克加入水中稀释,然后再与足量的氯化钡溶液反应,得到4.66g沉淀,沉淀是硫酸钡,物质的量是:$\frac{4.66g}{233g/mol}$=0.02mol,硫酸和氯化钡反应方程式为H2SO4+BaCl2=BaSO4+2HCl,根据方程式知n(BaSO4)=n(H2SO4)=0.02mol,则m(H2SO4)=0.02mol×98g/mol=1.96g,硫酸的质量分数=$\frac{{m}_{硫酸}}{{m}_{硫酸溶液}}$×100%;根据c=$\frac{1000ρω}{M}$计算该硫酸的物质的量浓度;
(2)根据硫元素守恒,得到关系式:FeS2~2SO2~2SO2~2H2SO4,根据硫酸和黄铜矿的关系式计算黄铜矿的质量.
解答 解:(1)4FeS2+11O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+8SO2,根据硫元素守恒,得到关系式:FeS2~2SO2~2SO2~2H2SO4,取该硫酸2.45克加入水中稀释,然后再与足量的氯化钡溶液反应,得到4.66g沉淀,沉淀是硫酸钡,物质的量是:$\frac{4.66g}{233g/mol}$=0.02mol,硫酸和氯化钡反应方程式为H2SO4+BaCl2=BaSO4+2HCl,根据方程式知n(BaSO4)=n(H2SO4)=0.02mol,则m(H2SO4)=0.02mol×98g/mol=1.96g,硫酸的质量分数=$\frac{{m}_{硫酸}}{{m}_{硫酸溶液}}$×100%=$\frac{1.96g}{2.45g}$×100%=80%;
该硫酸的物质的量浓度为:c=$\frac{1000ρω}{M}$=$\frac{1000×1.73×80%}{98}$mol/L≈14.1mol/L,
答:该硫酸的质量分数为80%,物质的量浓度为14.1mol/L;
(2)根据硫元素守恒,得到关系式:FeS2~2SO2~2SO2~2H2SO4,
设消耗黄铜矿的质量为x,
FeS2~2SO2~2SO2~2H2SO4,
120 196
75%x 122.5t×80%
120:196=75%x:122.5t×80%
x=$\frac{122.5t×80%×120}{196×75%}$=80t
答:消耗80%黄铜矿的质量为80t.
点评 本题考查了化学方程式的计算,题目难度中等,明确发生反应原理为解答关键,注意掌握关系式法在化学计算中的应用,试题侧重考查学生的分析、理解能力及化学计算能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:多选题
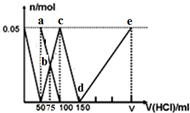
| A. | a点溶液中:c(HCO3-)+2c(H2CO3)+c(H+)=c(OH-) | |
| B. | b点所得溶液中有:c(Na+)>c(Cl-)>c(HCO3-)=c(CO32-)>c(OH-) | |
| C. | c点溶液中:c(Cl-)+c(HCO3-)+c(H2CO3)+c(CO32-)=0.75 mol/L | |
| D. | 原混合溶液中:n(CO32-):n(AlO2-)=1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④⑤ | B. | ②③④⑤ | C. | ①③④⑤ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、CH3COO-、Ca2+、Cl- | B. | Fe3+、Ag+、SO42-、NO3- | ||
| C. | Cu2+、H+、S2-、NO3- | D. | I-、Fe3+、K+、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 待测液中一定存在SO42-、Fe3+、Cl-,可能存在Na+ | |
| B. | 待测液中:c(Cl-)≥0.2mol•L-1 | |
| C. | 另取100mL待测液加入足量Ba(OH)2溶液,可得6.8g沉淀 | |
| D. | 另取100mL待测液加入足量AgNO3溶液,可得2.87g沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeBr2溶液中加入过量氯水:2Fe2++Cl2=2Fe3++2Cl- | |
| B. | 铁粉和FeCl3溶液反应:Fe+Fe3+=2Fe2+ | |
| C. | 铁粉和过量稀HNO3反应:Fe+NO3-+4H+=Fe3++NO↑+2H2O | |
| D. | Mg(HCO3)2溶液与过量NaOH溶液反应:Mg2++2HCO3-+2OH-=MgCO3↓+CO32-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
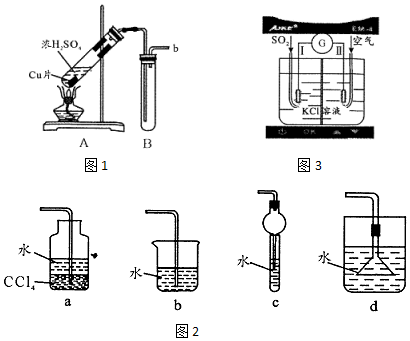
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | NH4+、Al3+、SO42-、NO3- | B. | Al3+、K+、Cl-、S2- | ||
| C. | NH4+、Cl-、K+、CO32- | D. | Ca2+、NO3-、HCO3-、Al3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
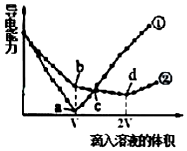 镁、钡是位于同一主族的活泼的金属元素.
镁、钡是位于同一主族的活泼的金属元素. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com