
分析 把明矾溶液中Al3+恰好沉淀完全时,生成沉淀的总的物质的量最大,即发生2KAl(SO4)2+3Ba(OH)2═K2SO4+3BaSO4↓+2Al(OH)3↓,
当a=b=0.5,c1=2,c2=3.6时,n(明矾)=0.5L×2mol/L=1mol,n(氢氧化钡)=0.5L×3.6mol/L=1.8mol;
根据反应方程式2KAl(SO4)2+3Ba(OH)2═K2SO4+3BaSO4↓+2Al(OH)3↓,K2SO4+2Al(OH)3+Ba(OH)2═2KAlO2+BaSO4↓+4H2O 分析计算.
解答 解:由方程式2KAl(SO4)2+3Ba(OH)2═K2SO4+3BaSO4↓+2Al(OH)3↓知,把明矾溶液中Al3+恰好沉淀完全时,生成沉淀的总的物质的量最大,
则$\frac{2}{a×{c}_{1}}=\frac{3}{b×{c}_{2}}$,解得b=$\frac{3a{c}_{1}}{2{c}_{2}}$L;
当a=b=0.5,c1=2,c2=3.6时,n(明矾)=0.5L×2mol/L=1mol,n(氢氧化钡)=0.5L×3.6mol/L=1.8mol;
由方程式2KAl(SO4)2+3Ba(OH)2═K2SO4+3BaSO4↓+2Al(OH)3↓知,当加入了1.5 mol Ba(OH)2时,生成沉淀的物质的量为1.5 mol+1 mol=2.5 mol,质量为1.5 mol×233 g/mol+1 mol×78 g/mol=427.5 g;
由方程式K2SO4+2Al(OH)3+Ba(OH)2═2KAlO2+BaSO4↓+4H2O 知,当继续滴加0.3 mol Ba(OH)2时,Al(OH)3沉淀的物质的量将减少0.3 mol×2=0.6 mol,BaSO4沉淀的物质的量增大0.3mol,沉淀的质量增加0.3 mol×233 g/mol-78 g/mol×0.6mol=23.1g,所以沉淀的总质量为427.5 g+23.1g=450.6g;
故答案为:b=$\frac{3a{c}_{1}}{2{c}_{2}}$;450.6g.
点评 本题考查了有关方程式的计算,硫酸铝钾和氢氧化钡反应有两种沉淀同时发生,要注意氢氧化铝能转化为可溶性的偏铝酸根离子,题中计算生成沉淀的物质的量和质量最大时b满足条件,结合方程式进行分析解答,难度较大.


 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案科目:高中化学 来源: 题型:选择题
| A. | ③⑤ | B. | ③⑥ | C. | ①② | D. | ⑤⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al3+、Fe3+、SO42- | B. | Na+、[Al(OH)4]-、CO32- | ||
| C. | Na+、[Al(OH)4]-、SO42-、CO32- | D. | Na+、Ba2+、[Al(OH)4]- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
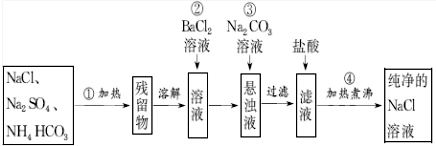
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
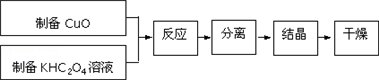
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应物总能量为679kj | |
| B. | 生成物总能量为431kj | |
| C. | 氢气和氯气反应生成2mol氯化氢气体,反应放出183kJ能量 | |
| D. | 氢气和氯气反应生成2mol氯化氢气体,反应吸收183kJ能量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com