
| A | B | C | D | |
| 方案 | 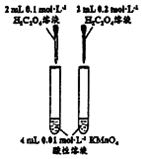 |  | 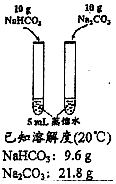 |  |
| 目的 | 探究浓度对化学反应速率的影响 | 制备氨气 | 室温下比较NaHCO3和Na2CO3的溶解度 | 探究温度对化学平衡的影响 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.只有浓度一个变量;
B.氯化铵与氢氧化钙加热生成氨气;
C.相同条件下,100g水中溶解的最大质量为溶解度;
D.只有温度一个变量.
解答 解:A.只有浓度一个变量,则可探究浓度对化学反应速率的影响,故A正确;
B.氯化铵与氢氧化钙加热生成氨气,则图中固体加热装置可制备氨气,故B正确;
C.相同条件下,100g水中溶解的最大质量为溶解度,图中均取10g固体、相同的水不能比较溶解度,故C错误;
D.只有温度一个变量,则可探究温度对化学平衡的影响,故D正确;
故选C.
点评 本题考查化学实验方案的评价,为高考常见题型和高频考点,把握反应速率、化学平衡、气体的制备及溶解度比较、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | MgF2的电子式: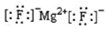 | |
| B. | 中子数为15的硅原子:${\;}_{14}^{29}$Si | |
| C. | 乙烯的结构简式:CH2CH2 | |
| D. | NH3•H2O 的电离方程式:NH3•H2O?NH4++OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 (1)已知在常温常压下:
(1)已知在常温常压下:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
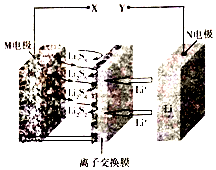 新型夹心层石墨烯锂硫二次电池的工作原理可表示为16Li+xS8$?_{充电}^{放电}$8Li2Sx,其放电时的工作原理如图所示,下列有关该电池的说法正确的是( )
新型夹心层石墨烯锂硫二次电池的工作原理可表示为16Li+xS8$?_{充电}^{放电}$8Li2Sx,其放电时的工作原理如图所示,下列有关该电池的说法正确的是( )| A. | 电池充电时X为电源负极 | |
| B. | 放电时,正极上可发生反应:2Li++Li2S4+2e-=2Li2S2 | |
| C. | 充电时,每生成1molS8转移0.2mol电子 | |
| D. | 离子交换膜只能通过阳离子,并防止电子通过 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 普通玻璃、水泥成分中都含有这三种元素 | |
| B. | 自然界中存在单质硅 | |
| C. | 氧元素与另外两种元素形成的二元化合物都能与NaOH的浓溶液反应 | |
| D. | 电解熔融状态的SiO2和A12O3可以制得Si、A1,且都有氧气生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 温度 n(CO) 时间 | 0 | 10 | 20 | … | 40 | 50 |
| T1 | 1.0 | 0.7 | 0.5 | … | 0.25 | 0.25 |
| T2 | 1.0 | 0.65 | 0.4 | … | 0.28 | 0.28 |
| A. | T1温度下平衡后恒容再充入0.5molCO,重新平衡后CO总的转化率与H2相等 | |
| B. | T1温度下10-20sH2的反应速率为0.04mol•L-1•s-1 | |
| C. | 该反应的△Η>0 | |
| D. | T2温度下平衡后恒定压强不变充入0.28molCH3OH,CH3OH的体积分数不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2:1 | B. | 5:1 | C. | 7:2 | D. | 8:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 与浓硫酸共热消去 | B. | 与浓氢溴酸卤代 | ||
| C. | 铜催化氧化 | D. | 与戊酸催化酯化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com