
 ����ȼ�ϵ���Ƿ�����ɫ��ѧ��������ͷ���װ�ã���ͼΪ���ʾ��ͼ���õ�ص缫�����һ��ϸС�IJ��ۣ����������������ǿ�������ȶ�����ش�
����ȼ�ϵ���Ƿ�����ɫ��ѧ��������ͷ���װ�ã���ͼΪ���ʾ��ͼ���õ�ص缫�����һ��ϸС�IJ��ۣ����������������ǿ�������ȶ�����ش����� ��1��ԭ����ǽ���ѧ��ת��Ϊ���ܵ�װ�ã�ԭ��طŵ�ʱ�����ӴӸ����ص�������������
��2��������ȼ��ʧ���ӷ�����ԭ��Ӧ�������������õ����������������ӣ�
��3���μӷ�Ӧ������Ũ������Ӧ���ʼӿ죮
��� �⣺��1����װ���ǰѻ�ѧ�����е�����ת��Ϊ���ܣ������ǻ�ѧ��ת��Ϊ���ܣ���ԭ����У�������ʧ���ӣ������ϵõ��ӣ����ӵ������ǴӸ������������������� ��a��b��
�ʴ�Ϊ����ѧ��ת��Ϊ���ܣ�a��b��
��2�����Ի����У��÷�Ӧ�и���������ʧ�������������ӣ��缫��ӦʽΪH2+2OH--2e-�T2H2O�������������õ����������������ӣ��缫��ӦʽΪ2H2O+O2+4e-�T4OH-���ʴ�Ϊ��2H2+4OH--4e-�T4H2O��2H2O+O2+4e-�T4OH-��
��3���缫����Ʋ��ۣ������˵缫��λ�������H2��O2�ķ�������ʹ��Ӧ���Ũ������Ӧ���ʼӿ죬
�ʴ�Ϊ������缫��λ�������H2��O2�ķ��������ӿ�缫��Ӧ���ʣ�
���� ���⿼�黯ѧ��Դ�Ĺ���ԭ������Ŀ�ѶȽϴ�ע��ԭ��ص缫��Ӧʽ����д��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | HR | B�� | H2R | C�� | RH3 | D�� | RH4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ������ | Fe��OH��3 | Fe��OH��2 | Co��OH��2 | Al��OH��3 | Mn��OH��2 |
| ��ȫ������pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| ���� | Fe��OH��3 | Fe��OH��2 | Zn��OH��2 | Mn��OH��2/Mn��OH��3 |
| ��ʼ����pH | 2.7 | 7.6 | 5.7 | 8.3 |
| ��ȫ����pH ��c��1.0��10-5mol/L�� | 3.7 | 9.6 | 8.0 | 8.8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
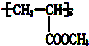 �����ִ��Ľṹ��ʽΪ��������
�����ִ��Ľṹ��ʽΪ��������| A�� | CH2�TCHCH2OH | B�� | CH3CH2OH | C�� | CH3CH��OH��CH2OH | D�� | CH2ClCHClCH2OH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | ������ӦΪAg-e-=Ag+ | |
| B�� | �ŵ�ʱ������Ĥ�����Һ���д�����ɫ�������� | |
| C�� | ����·��ת��0.1mole-ʱ��ͨ������Ĥ��������Ϊ0.2mol | |
| D�� | ��KCl��Һ�������ᣬ�����ܷ�Ӧ��ı� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | K 1s22s22p63s23p64s1 | B�� | Mg2+ 1s22s22p6 | ||
| C�� | F- 1s22s22p5 | D�� | Br 1s22s22p63s23p63d104s24p5 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com