
【题目】下列溶液中导电性最强的是( )
A. 1 L 0.1 mol/L AlCl3溶液 B. 0.1 L 0.1 mol/L H2SO4溶液
C. 0.5 L 0.15 mol/L盐酸 D. 2 L 0.1 mol/L H2SO3溶液
【答案】A
【解析】
溶液的导电能力与自由移动离子的浓度成正比,离子浓度越大,溶液的导电能力越强,
结合电离方程式或物质的构成解答该题。
A. AlCl3为强电解质,其电离方程式为:AlCl3 = Al3++3Cl-,Al3+有极少部分会发生水解,则0.1 mol/L AlCl3溶液阴阳离子总浓度约等于0.4 moL/L;
B. H2SO4强电解质,其电离方程式为:H2SO4 = 2H++SO42-,则0.1 mol/L H2SO4溶液中阴阳离子总浓度等于0.3 mol/L;
C. HCl为强电解质,其电离方程式为:HCl = H++ Cl-,则 0.15 mol/L盐酸中阴阳离子总浓度等于0.3mol/L;
D. H2SO3为弱电解质,其电离方程式为:H2SO3![]() 2H++SO32-,则0.1 mol/L H2SO3溶液不能完全电离,则阴阳离子总浓度略小于0.2mol/L;
2H++SO32-,则0.1 mol/L H2SO3溶液不能完全电离,则阴阳离子总浓度略小于0.2mol/L;
则可以看出离子浓度最大的为A,导电性最强,故A项正确;
答案选A。


 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源: 题型:
【题目】由乙烯和其他无机原料合成环状酯E和髙分子化合物H的示意图如图所示:
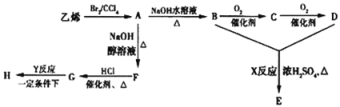
请回答下列问题:
(1)写出以下物质的结构简式:B______,G_______
(2)写出以下反应的反应类型:X_____,Y______.
(3)写出以下反应的化学方程式:A→B:_______
(4)若环状酯E与NaOH水溶液共热,则发生反应的化学方程式为______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产生活、环境保护、资源利用等密切相关,下列说法正确的是
A. 大米、玉米、小麦中的淀粉经水解可变成乙醇
B. 利用二氧化碳制造全降解塑料,可以缓解温室效应
C. 测定氢氧化钠的熔点时,可以将氢氧化钠固体放入石英坩埚中高温加热
D. 海洋中含有丰富的矿产资源,仅利用物理方法可以获得![]() 和
和![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合物浆液含有Al(OH)3、MnO2和少量Na2CrO4,。考虑到胶体的吸附作用使Na2CrO4不易完全被水浸出,某研究小组利用设计的电解分离装置,使浆液分离成固体混合物和含铬元素溶液,并回收利用。回答Ⅰ和Ⅱ中的问题。

Ⅰ.固体混合物的分离和利用(流程图中的部分分离操作和反应条件未标明)
(1)反应①所加试剂NaOH的电子式为_________。B→C的反应条件为__________,C→Al的制备方法称为______________。
(2)该小组探究反应②发生的条件。D与浓盐酸混合,不加热,无变化,加热有Cl2生成,当反应停止后,固体有剩余,此时滴加硫酸,又产生Cl2。由此判断影响该反应有效进行的因素有(填序号)___________。
a.温度 b.Cl的浓度 c.溶液的酸度
Ⅱ.含铬元素溶液的分离和利用
(3)用惰性电极电解时,![]() 能从浆液中分离出来的原因是__________;阴极室生成的物质为___________(写化学式)。
能从浆液中分离出来的原因是__________;阴极室生成的物质为___________(写化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上,常用O2氧化HCl转化成Cl2,提高效益,减少污染。反应为:4HCl(g)+O2(g)![]() 2Cl2(g)+2H2O(g)。一定条件下,测得数据如下:
2Cl2(g)+2H2O(g)。一定条件下,测得数据如下:
t/min | 0 | 2.0 | 4.0 | 6.0 | 8.0 | 10.0 |
c(Cl2)/10-3molL-1 | 0 | 1.8 | 3.7 | 5.4 | 7.2 | 7.2 |
下列说法错误的是( )
A.条件不变时,12min时v正(Cl2)=v逆(H2O)
B.2.0~4.0min内的平均反应速率大于6.0~8.0min内的
C.0~8.0min内HCl的平均反应速率为1.8mol·L-1·min-1
D.加入高效催化剂,达到平衡所用时间小于8.0min
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KMnO4是实验室中常用的一种试剂。回答下列问题:
(1)K+的结构示意图为___。
(2)在酸性高锰酸钾溶液中滴加过量的草酸(H2C2O4,弱酸)溶液,振荡,溶液紫色变无色。发生的化学反应为2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O,若将该反应设计成原电池,则负极反应式为___。
(3)在10mL0.1mol·L-1KMnO4溶液(含稀硫酸)中加入15mL0.5mol.L-1草酸溶液,收集到的CO2的量与时间的关系如图所示。

AB段反应速率增大的原因可能是___(填字母)。
a.该反应是放热反应
b.反应物浓度增大
c.K2SO4起催化作用
d.MnSO4起催化作用
(4)为了探究外界条件对化学反应速率的影响,设计如下方案:
实验 | 0.1mol·L-1KMnO4/mL | 0.5mol·L-1H2C2O4/mL | 0.1mol·L-1H2SO4/mL | 水浴 温度/℃ | 蒸馏水 /mL | 褪色时间 /min |
I | 5.0 | 15.0 | 5.0 | 35 | 0 | t1 |
II | 5.0 | 10.0 | 5.0 | 35 | V | t2 |
III | 5.0 | 15.0 | 3.0 | 35 | 2.0 | t3 |
IV | 5.0 | 15.0 | 5.0 | 45 | 0 | t4 |
①V=___。
②该实验方案不能探究对反应速率有影响的因素是___。
A.浓度 B.酸度 C.温度 D.催化剂
③若测得结果:t4<t1,则实验结论是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中投入1molCH3COOCH3(l)和1molC6H13OH(l)发生反应:CH3COOCH3(l)+C6H13OH(l) ![]() CH3COOC6H13(l)+CH3OH(l)。测得体系中CH3OH的物质的量与时间的变化关系如图所示。
CH3COOC6H13(l)+CH3OH(l)。测得体系中CH3OH的物质的量与时间的变化关系如图所示。

回答下列问题:
(1)CH3COOCH3的一种同分异构体属于酸,它的结构简式为___。
(2)己醇(C6H13OH)中,含3个甲基的结构有___种(不考虑立体异构)。
(3)M点:正反应速率___逆反应速率(填“大于”“小于”或“等于”,下同)。N点正反应速率___M点逆反应速率。
(4)上述反应在0~5min内CH3COOCH3的平均反应速率为___mol·min-1。
(5)上述反应达到平衡时,C6H13OH的转化率为___%。
(6)N点混合物中CH3COOC6H13的物质的量分数为___%。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学欲用浓H2SO4配制480mL 0.2mol·L-1的稀H2SO4。
(1)需要量取98%密度为1.84g·cm-3的浓硫酸________mL。
(2)配制时,必须使用的仪器有______(填代号),还缺少的仪器是_________、_________。
①烧杯;②10mL量筒;③20mL量筒;④托盘天平(带砝码);⑤玻璃棒
(3)配制时,该实验两次用到玻璃棒,其作用分别是________________、_______________。
(4)配制过程中出现以下情况,对所配溶液浓度有何影响(填“偏高”、“偏低”、“无影响”)。
①容量瓶没有干燥________,
②用量筒量取98%的硫酸溶液时俯视________,
③溶液转移到容量瓶后,未进行洗涤操作_________ ,
④定容时俯视容量瓶__________,
⑤如果加水超过了刻度线,取出水使液面恰好到刻度线________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有NO2、O2的混合气体12 mL,通入足量水中,充分反应后剩余气体2 mL(同温同压下),则原混合气体中氧气的体积是( )
A.1.3 mLB.2.4 mLC.3 mLD.4 mL或1.2 mL
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com