
【题目】下列属于非电解质的是
A.石墨B.一水合氨C.酒精D.氯化钠溶液
 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
【题目】化学在生产和日常生活中有着重要的应用.下列说法不正确的是( )
A. 工业上可用铝热反应大规模炼铁
B. SO2常用于纸张等植物纤维的漂白
C. Si是重要的半导体材料
D. 电解熔融MgCl2,可制得金属镁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 常温常压下,11.2 L N2为0.5 mol
B. 标准状况下,22.4 L H2和O2的混合气体所含分子数为NA
C. 标准状况下,18 g H2O的体积是22.4 L
D. 1 mol SO2的体积一定为22.4 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有含NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂将其转化为相应的沉淀或固体,从而实现Cl-、SO42-和NO3-的相互分离。实验流程可用下图表示:

请回答下列问题:
(1)写出实验流程中下列物质的化学式:
试剂X:______________,沉淀B:___________________。
(2)实验流程中加入过量的Na2CO3的目的是 _______________________________________。
(3)实验方案得到的溶液3中肯定含有________________(填化学式)杂质;为了解决这个问题,可以向溶液3中加入适量的__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W、R、M为元素周期表中前四周期的元素,其原子序数依次增大。X与W、Z与R是分别同族元素;X原子的第一电离能小于同周期前一族元素的原子;Z元素基态原子的核外有3个未成对电子;M元素的单质化学性质稳定,耐腐蚀,其单质及合金是一种优良的航天、航空材料,M的基态原子核外有2个未成对电子。请回答下列问题:
⑴NaZ3可应用于汽车安全气囊,当汽车发生碰撞时,气囊中的NaZ3迅速分解产生大量Z 的单质气体,从而使安全气囊瞬间充气弹出,减轻了乘员受到的伤害。基态Z原子价电子的电子排布图为_____________。与Z3-互为等电子体的分子的化学式为______________(写一个即可),Z3-的空间构型是__________。
⑵W元素可形成[WF6]3-、[WCl4]-配离子,而X只能形成[XF4]-配离子,由此可知决定配合物中配位数多少的因素之一是________________;
⑶已知Y的最高价含氧酸根离子与Na+、K+、NH4+形成的酸式盐溶解度都小于其正盐的溶解度,原因是HCO3-之间以________(填作用力)作用形成长链,减小了HCO3-与水分子之间的作用导致溶解度降低;
⑷R元素通常有白、红、黑三种颜色的单质,其中最稳定的同素异形体G在通常状态下是一种黑色有金属光泽的晶体,G在储能、电子和光伏发电等领域有着广泛的应用前景,是一种比石墨烯更优秀的新型材料。晶体G具有与石墨类似的层状结构,如图一所示。下列有关G的说法正确的是_______________;
A.G中R原子杂化方式为sp3杂化
B.G中层与层之间的作用力是配位健
C.与石墨类似,G的每一层中R原子都在同一平面上
D.R元素三种常见的单质中,G的熔沸点最高
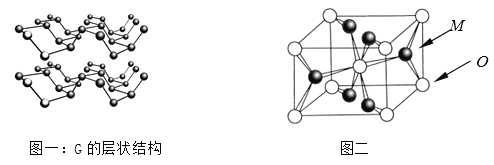
⑸M与O形成的离子晶体在自然界中存在三种形态,其中金红石型是三种形态中最稳定的一种,其晶胞如图二所示,则M、O配位数之比为________;影响离子晶体结构类型的因素有_____________、____________、键性因素。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列几个反应的化学方程式:① 2KI+Cl2=2KCl+I2、② 2FeCl2+Cl2=2FeCl3、③ 2FeCl3+2HI=2FeCl2+I2+2HCl,下列有关物质的氧化性的强弱排列顺序中正确的是
A.Cl2>Fe3+>I2 B.Cl2>I2>Fe3+
C.Fe3+>Cl2>I2 D.Fe3+>I2>Cl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下有三组混合物:①氯化钠和水;②硫酸钡和水;③煤油和水。分离以上混合液的正确方法依次是( )
A. 分液、萃取、蒸馏 B. 蒸发、过滤、分液 C. 分液、蒸发、萃取 D. 蒸馏、萃取、分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 下列各组元素中按微粒半径递增顺序排列的是 ( )
A. Li K Na B. Ba2+Ca2+Mg2+ C. Ca2+K+Cl- D. N O F
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com