
| A、H2(气)+Br2(气)?2HBr(气) (正反应为放热反应) |
| B、N2(气)+3H2(气)?2NH3(气) (正反应为放热反应) |
| C、2SO3(气)?2SO2(气)+O2(气) (正反应为吸热反应) |
| D、4NH3(气)+5O2(气)?4NO(气)+6H2O(气) (正反应为放热反应) |
| m总 |
| n总 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 2,3,5,5-四甲基-4,4-二乙基己烷 |
B、 2-甲基-3-丁烯 |
C、 4,7-二甲基-3-乙基壬烷 |
D、 1,3,5-三硝基苯酚 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、①是其他条件一定时,反应速率随温度变化的图象,正反应△H>0 |
| B、②是在平衡体系的溶液中溶入少量KCl晶体后化学反应速率随时间变化的图象 |
| C、③是在有无催化剂存在下建立的平衡过程图象,b是使用催化剂时的曲线 |
| D、④是一定条件下,向含有一定量A的容器中逐渐加入B时的图象,压强p1>p2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、容器Ⅰ、Ⅱ中正反应速率相同 |
| B、容器Ⅰ、Ⅲ中反应的平衡常数相同 |
| C、容器Ⅰ中CO的物质的量比容器Ⅱ中的多 |
| D、容器Ⅰ中CO的物质的量比容器Ⅱ中的少 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、2CH3CH2OH+O2
| |||
B、 +HNO3 +HNO3
 +H2O +H2O | |||
C、CH3CH2OH+CH3COOH
| |||
D、CH4+Cl2
|
查看答案和解析>>
科目:高中化学 来源: 题型:
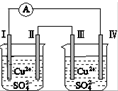
| A、电子移动:电极Ⅰ→电极Ⅳ→电极Ⅲ→电极Ⅱ |
| B、电极Ⅰ发生还原反应 |
| C、电极Ⅳ逐渐溶解 |
| D、电极Ⅲ的电极反应:Cu-2e-═Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
| 加热、加压 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com