
| c(标准)×V(标准) |
| V(待测) |
| m(Na2S2O3) |
| m(样品) |
| c(标准)×V(标准) |
| V(待测) |
| c(标准)×V(标准) |
| V(待测) |
| c(标准)×V(标准) |
| V(待测) |
| c(标准)×V(标准) |
| V(待测) |
| 1 |
| 10 |
| 2amol/L×b×10-3L×158g/mol | ||
|
| 3.16ab |
| w |
| 3.16ab |
| w |


 黄冈创优卷系列答案
黄冈创优卷系列答案科目:高中化学 来源: 题型:
| A、由mXa+与nYb-得,m+a=n-b |
| B、X2-还原性一定大于Y-的还原性 |
| C、X、Y一定不是同一周期 |
| D、若原子半径X>Y,则气体的稳定性:HmX>HnY |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验序号 | 加入水的质量/g | NaCl质量/g | 未溶的NaCl质量/g |
| ① | 10 | 4 | 2 |
| ② | 20 | 4 | 0 |
| ③ | 30 | 4 | 0 |
| A、实验①所得溶液为饱和溶液 |
| B、实验②所得溶液为饱和溶液 |
| C、20℃时NaCl的溶解度为2g |
| D、实验③所得溶液的溶质质量分数为13.3% |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、利用太阳能等清洁能源代替化石燃料,有利于节约资源,保护环境 |
| B、水电站把机械能转化为电能,而核电站把化学能转化为电能 |
| C、化石燃料和植物燃料燃烧时放出的热量均来源于太阳能 |
| D、植物通过光合作用将C02和H20转化为葡萄糖是太阳能转变为化学能的过程 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 Ni(CO)4(g)
Ni(CO)4(g)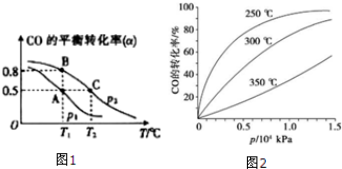
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、读取盐酸体积时,开始仰视读数,滴定结束时俯视读数 |
| B、滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥 |
| C、酸式滴定管在滴定前有气泡,滴定后气泡消失 |
| D、酸式滴定管未用标准盐酸润洗就直接注入标准盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| c(OH-) |
| c(NH3?H2O) |
+ 4 |
2- 4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com