
| A.0.8 | B.1.3 | C.1.6 | D.3.1? |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
| A.12:3.25 | B.3.25:12 | C.1:1 | D.6:1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.-1780kJ/mol | B.-1220 kJ/mol | C.-450 kJ/mol | D.+430 kJ/mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.-1648.8KJ/mol | B.-824.4KJ/mol | C.+1648.8KJ/mol | D.-744.7KJ/mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.2Q1+Q2>Q3 | B.Q1+Q2>2Q3 | C.2Q1+Q2<4Q3 | D.2Q1+Q2<2Q3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 O2(g)=H2O(g) △H1
O2(g)=H2O(g) △H1 N2(g)+O2(g)=NO2(g) △H2
N2(g)+O2(g)=NO2(g) △H2  N2(g)+
N2(g)+ H2(g)=NH3(g) △H3
H2(g)=NH3(g) △H3  O2(g)=2NO2(g)+3H2O(g)的△H为
O2(g)=2NO2(g)+3H2O(g)的△H为| A.2△H1+2△H2-2△H3 | B.△H1+△H2-△H3 |
| C.3△H1+2△H2+2△H3 | D.3△H1+2△H2-2△H3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CH3OH(g)+H2O(g)△H1
CH3OH(g)+H2O(g)△H1 CH3OH(g) △H2
CH3OH(g) △H2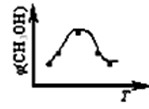
| A.升高温度 | B.增加CO2的量 |
| C.充入He,使体系总压强增大 | D.按原比例再充入CO2和H2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com