
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、实验室从海带提取单质碘的方法是:取样→灼烧→溶解→过滤→萃取 |
| B、石英只能用于生产光导纤维 |
| C、“盐卤点豆腐”利用了胶体的性质 |
| D、CO2、NO2、SO2都会导致酸雨的形成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
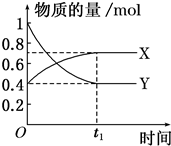
| A、整个反应阶段平均速率:醋酸>盐酸 |
| B、反应所需时间:醋酸>盐酸 |
| C、参加反应的锌的质量:盐酸<醋酸 |
| D、开始反应速率:盐酸>醋酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 放电 |
| 充电 |
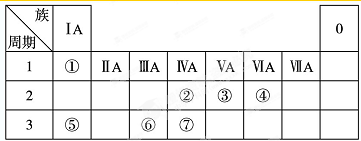
| A、③ | B、② | C、②和④ | D、①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物.已知:
如图,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物.已知:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 序号 | 氧化剂 | 还原剂 | 其他反应物 | 氧化产物 | 还原产物 |
| ① | Cl2 | FeBr2 | Cl- | ||
| ② | KMnO4 | H2O2 | H2SO4 | O2 | Mn2+ |
| ③ | KClO3 | 浓盐酸 | Cl2 |
| A、表中①组反应可能有一种或两种元素被氧化 |
| B、表中②组反应的离子方程式是2MnO4-+3H2O2+6H+═2Mn2++4O2↑+6H2O |
| C、表中③组反应的还原产物是KCl,电子转移数目是6e- |
| D、氧化性强弱比较:KClO3>Fe3+>Cl2>Br2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com