
(10分)根据要求回答下列各题:
(Ⅰ)现有①Na2O ②SO3 ③铁 ④蔗糖 ⑤冰醋酸(纯醋酸晶体) ⑥KNO3晶体 ⑦氢氧化钠溶液等物质,请填空回答(填序号):以上物质在常温下
(1)能导电的是 ; (2)属于非电解质的是 ;
(3)属于电解质的是 ;(4)属于弱电解质的是 。
(Ⅱ)写出下列反应的化学方程式:
(1)有H2O参加的化合反应: ;(2) 有H2O生成的分解反应: ;
(3)有HCl生成的置换反应: ;(4) 有HCl参加的复分解反应: 。
(Ⅲ)某有机混合物4.6 g完全燃烧,将燃烧后的混合物通入过量的澄清石灰水,石灰水共增重14.2 g,经过滤得到20g沉淀.该有机样品可能是:
A.C2H6O2
B.CH4和C2H6的混合物
C.C2H6O和C3H8O3的混合物
D.CH4O和C3H8O的混合物
(共10分)(Ⅰ)(4分子,多选项错1个不得分)(1) ③⑦ (2) ②④ (3) ①⑤⑥ (4) ⑤
(Ⅱ)(4分)(1)Na2O+H2O=2NaOH 等 (2)酸、碱、盐等分解反应均可
(3)2HI+Cl2=2HCl+I2 等 (4)HCl+NaOH=NaCl+H2O等 (Ⅲ)(2分)D
【解析】
试题分析:(Ⅰ)(1)③铁⑦氢氧化钠中含有自由移动的粒子,能导电;故答案为:③⑦;
(2)②SO3④蔗糖在水溶液中和熔融状态下都不能够自身电离出离子,属于非电解质;故答案为:②④;
(3)①Na2O⑤冰醋酸(纯醋酸晶体) ⑥KNO3晶体在水溶液或是熔融态时能够电离出离子,属于电解质,故答案为:①⑤⑥;
(4)冰醋酸(纯醋酸晶体)在水溶液中部分电离,属于弱电解质,故答案为:⑤;
(Ⅱ)(1)有H2O参加的化合反应如:Na2O+H2O=2NaOH,故答案为:Na2O+H2O=2NaOH;
(2)有H2O生成的分解反应,如H2CO3=H2O+CO2↑(碱、盐等分解反应均可),故答案为:H2CO3=H2O+CO2↑(碱、盐等分解反应均可);
(3)有HCl生成的置换反应,如:2HI+Cl2=2HCl+I2,故答案为:2HI+Cl2=2HCl+I2;
(4)有HCl参加的复分解反应,如:HCl+NaOH=NaCl+H2O,故答案为:HCl+NaOH=NaCl+H2O;
(Ⅲ)20g沉淀为CaCO3,其物质的量为20g÷100g/mol=0.2mol,根据碳元素守恒可知,产生的二氧化碳为0.2mol,二氧化碳的质量为0.2mol×44g/mol=8.8g,其中碳元素质量为:0.2mol×12g/mol=2.4g,石灰水增重14.2g,所以有机物燃烧生成的水的质量为:14.2g-8.8g=5.4g,物质的量为5.4g÷18g/mol=0.3mol;氢元素质量为0.3mol×2×1g/mol=0.6g;有机样品共4.6gg,所以O元素物质的质量=4.6g-2.4g-0.6g=1.6g,氧原子物质的量为:1.6g÷16g/mol=0.1mol,即有机物中碳、氢、氧原子的物质的量之比为0.2mol:0.3mol×2:0.1mol=2:6:1,即最简式为C2H6O,最简式中H原子已经饱和C原子,只有D选项中CH4O和C3H8O按1:1混合时满足题意,故答案为:D。
考点:考查电解质的概念以及分类、化学反应类型的把握和反应方程式的书写以及有机物分子式的确定


科目:高中化学 来源:2015届浙江省高三9月月考化学试卷(解析版) 题型:选择题
下列实验设计及其对应离子方程式均正确的是( )
A.用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+===Cu2++2Fe2+
B.Na2O2与H2O反应制备O2:Na2O2+H2O===2Na++2OH-+O2↑
C.将氯气溶于水制备次氯酸:Cl2+H2O===2H++Cl-+ClO-
D.用浓盐酸酸化的KMnO4与H2O2反应,证明H2O2具有还原性:2MnO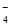 +6H++5H2O2===2Mn2++5O2↑+8H2O
+6H++5H2O2===2Mn2++5O2↑+8H2O
查看答案和解析>>
科目:高中化学 来源:2015届浙江省杭州市高三10月月考化学试卷(解析版) 题型:选择题
下列各组中的离子能在溶液中大量共存,向溶液中加入NaOH溶液时产生沉淀,且加入盐酸时放出气体的离子组是
A.OH-、Ba2+、NO3-、K+ B.Fe2+、Ca2+、Br-、NO3-
C.Na+、SO42-、Cu2+、Cl- D.CO32-、Cl-、Na+、Ba2+
查看答案和解析>>
科目:高中化学 来源:2015届浙江省杭州市高三10月月考化学试卷(解析版) 题型:选择题
下列氧化还原反应中,水作为氧化剂的是
A.CO+H2O(g)  CO2+H2 B.3NO2+H2O===2HNO3+NO
CO2+H2 B.3NO2+H2O===2HNO3+NO
C.2Na2O2+2H2O===4NaOH+O2↑ D.2F2+2H2O===4HF+O2
查看答案和解析>>
科目:高中化学 来源:2015届浙江省杭州市高三10月月考化学试卷(解析版) 题型:选择题
“纳米技术”广泛的应用于催化及军事科学中,“纳米技术”是指粒子直径在几纳米到几十纳米的材料。如将“纳米材料”分散到液体分散剂中,所得的混合物具有的性质是
A.能全部通过半透膜 B.能发生丁达尔现象
C.一定能导电 D.一定为悬浊液或乳浊液
查看答案和解析>>
科目:高中化学 来源:2015届浙江省慈溪市、余姚市高三上学期期中联考化学试卷(解析版) 题型:选择题
关于3Cl2 + 6KOH  KClO3 + 5KCl + 3H2O反应,以下说法错误的是
KClO3 + 5KCl + 3H2O反应,以下说法错误的是
A.Cl2既是氧化剂,又是还原剂
B.3 mol氯气参加反应转移5 mol电子
C.氧化产物的物质的量是还原产物的物质的量的5倍
D.每有1 mol原子被氧化的同时就有5 mol原子被还原
查看答案和解析>>
科目:高中化学 来源:2015届浙江省慈溪市、余姚市高三上学期期中联考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.制普通玻璃的主要原料是烧碱、石灰石、石英
B.晶体硅可用于制作半导体材料
C.实验室用带玻璃塞的试剂瓶保存氢氧化钠溶液
D.光导纤维的主要成份是硅
查看答案和解析>>
科目:高中化学 来源:2015届浙江省高三上学期第二次质量检测化学试卷(解析版) 题型:填空题
(8分)污染与环境保护已经成为现在我国最热门的一个课题,污染分为空气污染,水污染,土壤污染等。
⑴为了减少空气中SO2的排放,常采取的措施有:
①将煤转化为清洁气体燃料。
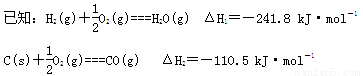
写出焦炭与水蒸气反应的热化学方程式______________________。
该反应的平衡常数表达式为K=_________。
②洗涤含SO2的烟气。以下物质可作洗涤剂的是________(选填序号)。
a.Ca(OH)2 b.CaCl2 c.Na2CO3 d.NaHSO3
⑵为了减少空气中的CO2,目前捕碳技术在降低温室气体排放中具有重要的作用,捕碳剂常用(NH4)2CO3,反应为:(NH4)2CO3(aq)+H2O(l)+CO2(g)=2NH4HCO3(aq),ΔH3
为研究温度对(NH4)2CO3捕获CO2效率的影响,在某温度T1下,将一定量的(NH4)2CO3溶液置于密闭容器中,并充入一定量的CO2气体(用氮气作为稀释剂),在t时刻,测得容器中CO2气体的浓度。然后分别在温度为T2、T3、T4、T5下,保持其他初始实验条件不变,重复上述实验,经过相同时间测得CO2气体浓度,其关系如图,则:
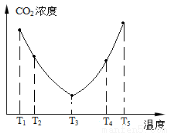
①ΔH3____0(填“>”、“=”或“<”)。
②在T4~T5这个温度区间,容器内CO2气体浓度变化趋势的可能原因有:___________________________;__________。
查看答案和解析>>
科目:高中化学 来源:2015届浙江省高三上学期第一次统练化学试卷(解析版) 题型:选择题
某溶液中含有AlO2-、SO 、SO
、SO 、Na+,向其中加入Na2O2后,溶液中浓度基本保持不变的离子是
、Na+,向其中加入Na2O2后,溶液中浓度基本保持不变的离子是
A.SO B.Na+ C.AlO2- D.SO
B.Na+ C.AlO2- D.SO
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com