
下列试剂中,可鉴别K2SO4、KCl、(NH4)2SO4、AlCl3四种物质的溶液的是
A.氨水 B.Ba(OH)2溶液 C.KOH溶液 D.AgNO3溶液
科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源:2013-2014学年江西省八校高三下学期联考理综化学试卷(解析版) 题型:实验题
绿矾(FeSO4?7H2O)是治疗缺铁性贫血的特效药。某学校的化学兴趣小组的同学对绿矾进行了如下的探究:
FeSO4?7H2O的制备
该化学兴趣小组的同学在实验室通过如下实验由废铁屑(含少量氧化铜、氧化铁等杂质)制备FeSO4·7H2O晶体:
①将5%Na2CO3溶液加入到盛有一定量废铁屑的烧杯中,加热数分钟,用倾析法除去
Na2CO3溶液,然后将废铁屑用水洗涤2~3遍。
②向洗涤过的废铁屑中加入过量的稀硫酸,控制温度在50~80℃之间至铁屑耗尽;
③趁热过滤,将滤液转入到密闭容器中,静置、冷却结晶;
④待结晶完毕后,滤出晶体,用少量冰水洗涤2~3次,再用滤纸将晶体吸干;
⑤将制得的FeSO4·7H2O晶体放在一个小广口瓶中,密闭保存。
请回答下列问题:
(1)实验步骤①的目的是 。
(2)实验步骤②明显不合理,理由是 。
(3)为了洗涤除去晶体表面附着的硫酸等杂质,实验步骤④中用少量冰水洗涤晶体,原因是 。
(二)探究绿矾(FeSO4·7H2O)热分解的产物
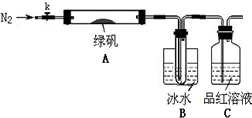
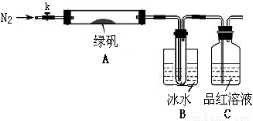 已知SO3的熔点是16.8°C,沸点是44.8°C,该小组设计如下图所示的实验装置(图中加热、夹持仪器等均省略):
已知SO3的熔点是16.8°C,沸点是44.8°C,该小组设计如下图所示的实验装置(图中加热、夹持仪器等均省略):
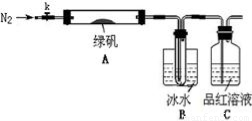
【实验过程】
①仪器连接后,检查装置A与B气密性;
②取一定量绿矾固体置于A中,通入N2以驱尽装置内的空气,关闭k,用酒精灯加热硬质玻璃管;
③观察到A 中固体逐渐变红棕色,B中试管收集到无色液体,C中溶液褪色;
④待A中反应完全并冷却至室温后,取少量反应后固体于试管中,加入硫酸溶解,取少量滴入几滴KSCN溶液,溶液变红色;
⑤往B装置的试管中滴入几滴BaCl2溶液,溶液变浑浊。
(4)实验结果分析
结论1:B中收集到的液体是?????????????????? ;
结论2:C中溶液褪色,可推知产物中有???? ?????????????? ;
结论3:综合分析上述实验③和④可推知固体产物一定有Fe2O3。
【实验反思】
(5)请指出该小组设计的实验装置的明显不足:??????????????????????????? 。
(6)分解后的固体中可能含有少量FeO,取上述实验④中盐酸溶解后的溶液少许于试管中,选用一种试剂鉴别,该试剂最合适的是?????????? 。
a.氯水和KSCN溶液???? b.酸性KMnO4溶液????? c.H2O2???? d.NaOH溶液
查看答案和解析>>
科目:高中化学 来源:2011-2012年福建省高一上学期期中考试化学试卷 题型:填空题
(11分)现有K 、O、S、H 四种元素,选用其中一种或几种元素可组成符合下列要求的物质(酸、酸性氧化物、盐、X)。
(1)完成下列转化:(用化学方程式表示)
①酸 → 盐: ;
②酸性氧化物 → 盐: ;
(2)X在水溶液中电离成K+ 、H+、SO42-,则X的化学式为 ,X属于 (填序号)
A.酸 B.碱 C.盐 D.氧化物
(3)设计两种实验方案(指出使用的试剂或方法)鉴别Na2SO4和X:
方案1: 。
方案2: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
(11分)现有K 、O、S、H 四种元素,选用其中一种或几种元素可组成符合下列要求的物质(酸、酸性氧化物、盐、X)。
(1)完成下列转化:(用化学方程式表示)
①酸 → 盐: ;
②酸性氧化物 → 盐: ;
(2)X在水溶液中电离成K+ 、H+、SO42-,则X的化学式为 ,X属于 (填序号)
A.酸 B.碱 C.盐 D.氧化物
(3)设计两种实验方案(指出使用的试剂或方法)鉴别Na2SO4和X:
方案1: 。
方案2: 。
查看答案和解析>>
科目:高中化学 来源:2011-2012年福建省福建师大附中高一上学期期中考试化学试卷 题型:填空题
(11分)现有K 、O、S、H 四种元素,选用其中一种或几种元素可组成符合下列要求的物质(酸、酸性氧化物、盐、X)。
(1)完成下列转化:(用化学方程式表示)
①酸 → 盐:  ;
;
②酸性氧化物 → 盐: ;
(2)X在水溶液中电离成K+ 、H+、SO42-,则X的化学式为 ,X属于 (填序号)
| A.酸 | B.碱 | C.盐 | D.氧化物 |
 鉴别Na2SO4和X:
鉴别Na2SO4和X:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com