
| A、用饱和NaHCO3溶液除去CO2中少量的HCl |
| B、NH4C1和I2的固体混合物可以用加热的方法分离 |
| C、植物油和水的混合物可以用分液的方法分离 |
| D、溴水中的溴单质可以用四氯化碳萃取 |


科目:高中化学 来源: 题型:
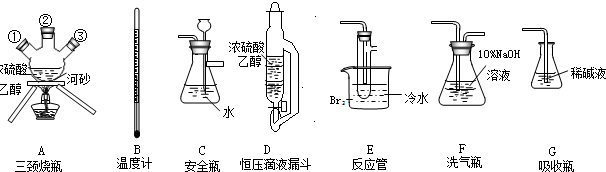
| 浓硫酸 |
| 170℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、离子反应的活化能几乎为零 |
| B、发生有效碰撞的分子一定是活化分子 |
| C、活化能对化学反应的反应热会产生影响 |
| D、活化能指活化分子多出其它反应物分子的那部分能量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com