
| A. | 蔗糖、硫酸钡和水分别属于非电解质、强电解质、弱电解质 | |
| B. | 甲醇、乙二醇(HOCH2CH2OH)互为同系物 | |
| C. | 除去CO2中混有的SO2:用饱和NaHCO3溶液洗气,再干燥 | |
| D. | 液溴易挥发,盛放在用水密封、玻璃塞塞紧的棕色试剂瓶中 |
分析 A、根据电解质、非电解质的概念和性质分析,蔗糖在熔融状态下和溶液中都不能导电,为非电解质,硫酸钡为强酸强碱盐,难溶于水,但溶于水的部分完全电离,为强电解质,水为弱电解质;
B、同系物的结构相似、相差n个CH2原子团,且官能团的种类与数目相同;
C、SO2与饱和NaHCO3溶液反应生成二氧化碳;
D、液溴易挥发,需液封.
解答 解:A、蔗糖在熔融状态下和溶液中都不能导电,为非电解质,硫酸钡为强酸强碱盐,难溶于水,但溶于水的部分完全电离,为强电解质,水为弱电解质,故A正确;
B、甲醇、乙二醇(HOCH2CH2OH)中官能团的种类相同,但数目不同,不是同系物,故B错误;
C、SO2与饱和NaHCO3溶液反应生成二氧化碳,能除去杂质且不引入新杂质,故C正确;
D、溴单质易挥发,应在盛溴的试剂瓶里加一些水来防止溴挥发,水封法保存,故D正确;
故选B.
点评 本题考查了物质的分类、分离、提纯等,明确常见物质的性质及混合物分离的方法即可解答,题目难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 还原剂 | B. | 氧化剂 | C. | 催化剂 | D. | 溶剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径W>X>Y | B. | W2Y的电子式为: | ||
| C. | 元素的金属性W<X | D. | W2Y2中既有离子键,又有共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCO3-、ClO-、K+、H+ | B. | Na+、Fe2+、NO3-、H+ | ||
| C. | K+、Mg2+、Cl-、SO42- | D. | OH-、NH4+、Cl-、SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
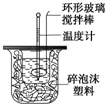 利用下图装置测定中和热的实验步骤如下:
利用下图装置测定中和热的实验步骤如下:| 温度 实验次数 | 起始温度t1℃ | 终止温度t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
| HCl | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 29.5 | |
| 2 | 27.0 | 27.4 | 27.2 | 32.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.2 | |
| 4 | 26.4 | 26.2 | 26.3 | 29.8 | |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 1 mol苯乙烯可以和4mol Br2发生加成反应 | |
| B. | 分子中所有原子可以在同一平面内 | |
| C. | 与HCl加成只生成一种产物 | |
| D. | 能使酸性KMnO4溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④⑥ | B. | ②③⑤ | C. | ④⑤ | D. | ②⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com