
| A. | 离子化合物中一定含有金属元素 | |
| B. | 分子晶体、原子晶体中一定含有共价键,离子晶体一定含有离子键 | |
| C. | 气态氢化物的稳定性:NH3>PH3>AsH3 | |
| D. | 正四面体结构的分子中的键角一定是109°28′ |
分析 A.铵盐是由非金属元素构成的离子化合物;
B.单原子分子中不存在共价键;
C.元素的非金属性越强,其氢化物越稳定;
D.正四面体结构的分子中的键角也可能是60°.
解答 解:A.铵盐是由非金属元素构成的离子化合物,所以离子化合物中不一定含有金属元素,故A错误;
B.单原子分子中不存在共价键,如稀有气体分子为单原子分子,分子中没有共价键,原子晶体中一定含有共价键,离子晶体一定含有离子键,故B错误;
C.元素的非金属性越强,其氢化物越稳定,非金属性:N>P>As,则气态氢化物的稳定性:NH3>PH3>AsH3,故C正确;
D.正四面体结构的分子中的键角也可能是60°,如白磷分子中键角是60°,不是109°28′,故D错误.
故选C.
点评 本题考查了化学键、离子化合物和共价化合物、氢化物稳定性比较、键角等,题目难度不大,侧重于基础知识的考查,注意相关知识的积累.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 0.01mol•L-1 KIO3 酸性溶液(含淀粉)的体积/mL | 0.01mol•L-1 Na2SO3 溶液的体积/mL | H2O的体积 /mL | 实验 温度 /℃ | 溶液出现蓝色时所需时间/s | |
| 实验1 | 5 | V1 | 35 | 25 | |
| 实验2 | 5 | 5 | 40 | 25 | |
| 实验3 | 5 | 5 | V2 | 0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙酸乙酯(乙酸):加入乙醇和浓硫酸,然后加热 | |
| B. | 碳酸钠固体(碳酸氢钠):加热至恒重 | |
| C. | FeCl2溶液(FeCl3、CuCl2):加入过量Fe粉充分搅拌,然后过滤 | |
| D. | 乙醇(水):加入新制的生石灰,然后蒸馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
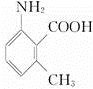 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
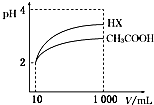 25℃时,三种酸的电离常数为:
25℃时,三种酸的电离常数为:| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数K | 1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属的导电性 | B. | 金属的延展性 | ||
| C. | 地壳中金属元素的含量 | D. | 金属冶炼的难易程度 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
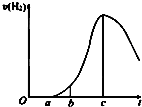 成都七中文艺青年小组进行了关于“活泼金属与酸反应”的实验,得出了一些有趣的想法,请你帮助他们,完成一些判断.将5.4g铝片投入500mL 0.5mol•L-1的硫酸溶液中,如图为反应产氢速率与反应时间的关系图.
成都七中文艺青年小组进行了关于“活泼金属与酸反应”的实验,得出了一些有趣的想法,请你帮助他们,完成一些判断.将5.4g铝片投入500mL 0.5mol•L-1的硫酸溶液中,如图为反应产氢速率与反应时间的关系图.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com