
| A. | Na+、K+、SO42-、HCO3- | B. | Na+、Fe3+、Cl-、SCN- | ||
| C. | Na+、K+、Cl-、NO3- | D. | Ca2+、Na+、ClO-、NO3- |
 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案科目:高中化学 来源: 题型:填空题
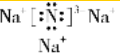 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10min内,Z的平均反应速率为0.02 mol•L-1•min-1 | |
| B. | 第10min时,X的物质的量浓度为0.8mol•L-1 | |
| C. | 10min内,消耗0.2 mol X,生成0.4 mol Z | |
| D. | 10min内,X和Y反应放出的热量为0.2a kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4Cl溶液、NaOH溶液、碱石灰 | B. | 浓氨水、NaOH固体、浓硫酸 | ||
| C. | NH4Cl固体、消石灰、碱石灰 | D. | 浓NaOH溶液、NH4Cl固体、浓硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由于碘在酒精中的溶解度大,所以可用酒精将碘水中的碘萃取出来 | |
| B. | 由于胶体微粒的直径比离子大,所以碘化钾混入淀粉中可用渗析法分离 | |
| C. | 可用冷却热的饱和氯化钾和氯化钠混合溶液的方法得到纯净的氯化钠晶体 | |
| D. | 水的沸点是100℃,酒精的沸点是78.5℃,所以可用直接加热蒸馏法使含水酒精变为无水酒精 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 总反应的速率由反应①的速率决定 | |
| B. | 反应④的焓变小于0 | |
| C. | HClI是上述总反应的催化剂 | |
| D. | 正反应活化能E${\;}_{{a}_{1}}$与逆反应活化能E${\;}_{{a}_{2}}$之差为a kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 简单氢化物的沸点:Y>R | |
| B. | 原子半径的大小顺序:Z>R>X>Y | |
| C. | 氧化物对应的水化物的酸性:R>X | |
| D. | 只含有Y、Z、R三种元素的化合物一定既含离子键又含共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 草莓棚中使用的“吊袋式二氧化碳气肥”的主要成分可以是碳酸钙 | |
| B. | 制作烟花的过程中常加入金属发光剂和发色剂使烟花放出五彩缤纷的颜色 | |
| C. | “梨花淡自柳深青,柳絮飞时花满城”中柳絮的主要成分和棉花的相同 | |
| D. | 《本草纲目》记载的“凡酸坏之酒,皆可蒸烧”的实验方法可用来分离乙酸和乙醇 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com