
下列有关原子结构和元素周期律的表述正确的是( )
①原子序数为15的元素的最高化合价为+3;
②ⅦA族元素是同周期中非金属性最强的元素;
③第二周期ⅣA族元素的原子核电荷数和中子数一定为6;
④原子序数为12的元素位于元素周期表的第三周期ⅡA族.
A. ①② B. ①③ C. ②④ D. ③④
考点: 原子结构与元素周期律的关系.
专题: 元素周期律与元素周期表专题.
分析: ①利用最外层电子数分析最高正化合价;②元素周期表中从左到右元素的非金属性在增强;③第二周期ⅣA族元素为C元素,核电荷数一定为6;④原子序数为12的元素为Mg元素.
解答: 解:原子序数为15的元素是P,最外层电子数为5,则最高化合价为+5价,故①错误;
在元素周期表中同一周期随原子序数递增非金属性逐渐增强,故②正确;
C的质子数为6,但中子数不一定为6,因C存在14C和13C等同位素,故③错误;
原子序数为12的元素为Mg,位于元素周期表的第三周期ⅡA族,故④正确.
故选C.
点评: 本题考查原子结构与元素周期律,熟悉元素在周期表在的位置及元素的性质即可解答,难度不大.


科目:高中化学 来源: 题型:
有人认为人体实际上是一架缓慢燃烧着的“高级机器”,人体在生命活动过程中也需要不断补充“燃料”,按照这种观点,人们通常摄入的下列物质不能看作“燃料”的是( )
|
| A. | 淀粉类物质 | B. | 水 | C. | 脂肪类物质 | D. | 蛋白质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
“魔棒”常被用于晚会现场气氛的渲染.其发光原理是利用H2O2氧化草酸二酯产生能量,该能量被传递给荧光物质后便发出荧光,草酸二酯(CPPO)结构简式如图.下列说法正确的是( )
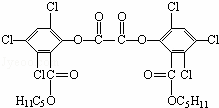
|
| A. | CPPO属于芳香烃 |
|
| B. | CPPO属于高分子化合物 |
|
| C. | 1mol CPPO与氢氧化钠稀溶液反应(假设苯环上卤素不水解),最多消耗6mol NaOH |
|
| D. | 1mol CPPO与氢气完全反应,需要氢气10mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
“柯达尔”是一种高聚物,其结构式为:

已知在一定条件下可以发生如下反应: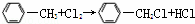
以石油产品(对二甲苯)为原料,合成“柯达尔”的方案如下:
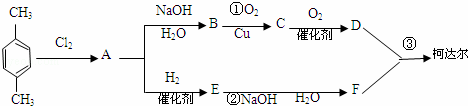
回答以下问题:
(1)指出反应的类型:A→B: ,A→E: .
(2)写出下列反应的化学方程式:B→C: ;E→F: ;D+F→柯达尔: .
查看答案和解析>>
科目:高中化学 来源: 题型:
已知短周期元素a、b、c、d、e的原子序数依次增大、其氢化物中a、b、c、d、e的化合价如表,下列说法不正确的是( )
元素 a b c d e
化合价 ﹣4 +1 ﹣4 ﹣2 ﹣1
A. 元素a、c、d的最高价氧化物都属于酸性氧化物
B. 元素c、d、e的氢化物稳定性和最高价氧化物对应水化物的酸性均依次增强
C. 元素周期表中,元素c位于金属和非金属分界线附近,其单质常用作光电池材料
D. 元素b、d、e的原子半径和离子半径均依次减小
查看答案和解析>>
科目:高中化学 来源: 题型:
可逆反应N2(g)+3H2(g)⇌2NH3(g)在体积不变的密闭容器中反应,达到平衡状态的标志是( )
①单位时间内生成n mol N2 的同时,生成3n mol H2
②断开1mol H﹣H键的同时断开2molN﹣H键
③用N2、H2、NH3的浓度变化表示的反应速率之比为1:3:2
④混合气体的压强不再改变
⑤混合气体的密度不再改变.
A. ②④ B. ①④ C. ①③④ D. ②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
如图是可逆反应X2+3Y2⇌2Z2 在反应过程中的反应速率V与时间(t)的关系曲线,下列叙述正确的是( )

A. t1时,只有正方向反应
B. t2时,反应到达限度
C. t2﹣t3,反应不再发生
D. t2﹣t3,各物质的浓度不再发生变化
查看答案和解析>>
科目:高中化学 来源: 题型:
食品香精菠萝酯的生产路线(反应条件略去)如下:

下列叙述错误的是( )
A. 步骤(1)产物中残留的苯酚可用FeCl3溶液检验
B. 苯酚和菠萝酯均可与酸性KMnO4溶液发生反应
C. 苯氧乙酸和菠萝酯均可与NaOH溶液发生反应
D. 步骤(2)产物中残留的丙烯醇可用溴水检验
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,在1L容器中,a mol SO2与b mol O2反应2SO2+O2⇌2SO3达到平衡时有c mol SO2发生了反应,则:
(1)生成 mol SO3;
(2)O2的转化率为
(3)平衡时容器内气体总物质的量为 ()mol
(4)平衡体系中SO3的百分含量(体积比) ×100%
(5)平衡浓度[SO2]= mol•L﹣1.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com