

| ||
| ||
| ||
| ||


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、Ca(ClO)2溶液中:c(ClO-)>c(Ca2+)>c(OH-)>c(H+) |
| B、等体积、等物质的量浓度的NaX和弱酸HX混合:c(Na+)-c(X-)>c(OH-)>c(H+) |
| C、常温下,将25mL0.2mol/L的盐酸与l00mL0.lmol/L的氨水混合,所得溶液中:c(NH4+)>c(Cl-)>c(NH3?H2O)>c(OH-)>c(H+) |
| D、将0.lmol/L的Na2S溶液与0.lmol/L的NaHS溶液等体积混合,所得溶液中:c(S2-)+2c(OH一)═2c(H+)+c(HS-)+3c(H2S) |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、MgO+H2
| ||||
B、Fe3O4+4CO
| ||||
C、2NaCl(熔融)
| ||||
D、2 HgO
|
查看答案和解析>>
科目:高中化学 来源: 题型:
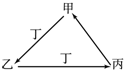 甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下图转化关系.下列有关物质的推断正确的是( )
甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下图转化关系.下列有关物质的推断正确的是( )| A、若甲为N2,则丁可能是O2 |
| B、若甲为Fe,则丁可能是Cl2 |
| C、若甲为AlCl3,则丁可能是NH3 |
| D、若甲为NaHCO3,则丁可能是HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
 的下列叙述中,正确的是( )
的下列叙述中,正确的是( )| A、可能在同一平面上的原子最多有20个 |
| B、12个碳原子不可能都在同一平面上 |
| C、所有的原子都在同一平面上 |
| D、除苯环外的其余碳原子有可能都在一条直线上 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| Fe3+ | Cu2+ | Cr3+ | |
| 开始沉淀pH | 2.1 | 4.7 | 4.3 |
| 完全沉淀pH | 3.2 | 6.7 | a |
| 3 | 63 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 加热前质量 | 加热后质量 | |
| m1(容器) | m2(容器+晶体) | m3(容器+无水硫酸铜) |
| 5.400g | 7.900g | 7.100g |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度/℃ | 700 | 800 | 830 | 1000 | 1200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
| 1 |
| 2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com