
为了除去食盐水中的![]() ,有以下操作步骤:
,有以下操作步骤:
①过滤
②加入稍过量的![]() 和NaOH溶液
和NaOH溶液
③加入稍过量的![]() 溶液
溶液
④加入盐酸调pH值至中性.其操作程序正确的是
[ ]
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:高中化学习题 题型:043
为了除去饱和食盐水中的![]() 和
和![]() 等杂离子得到精制的
等杂离子得到精制的![]() 溶液,以作为氯碱工业的原料.具体精制提纯的操作有:①过滤;②加入稍过量的
溶液,以作为氯碱工业的原料.具体精制提纯的操作有:①过滤;②加入稍过量的![]() 溶液;③加入稍过量的稀盐酸;④加入稍过量的
溶液;③加入稍过量的稀盐酸;④加入稍过量的![]() 溶液;⑤加入稍过量的
溶液;⑤加入稍过量的![]() 溶液.试通过分析回答以下各问:
溶液.试通过分析回答以下各问:
(1)食盐水提纯的正确操作顺序(填写代号)应为________.
(2)简要说明各步操作的化学原理,并写出相关的离子反应方程式.
查看答案和解析>>
科目:高中化学 来源:2013-2014学年浙江省六市六校联盟高考模拟考试理科综合化学试卷(解析版) 题型:填空题
下图是两座工厂的主要生产流程以及它们之间的生产关系
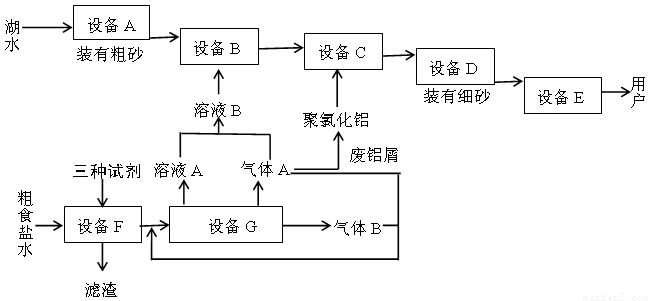
回答下列问题:
(1)与上图中“设备A”的作用相当的实验装置是???????? 。

(2)“溶液B”也可以用下列物质中的什么物质代替?????? 。
a.KAl(SO4)2·12H2O????? b.ClO2??????? c.大量O3????? d.K2Cr2O7?????? e.活性炭
(3)聚氯化铝在生产过程中作??????? 剂,其作用是????????????? ,可用离子方程式表示其化学原理如下(用Al3+代表聚氯化铝):??????????????????????? 。
(4)上图中下方的工厂主要生产两种气体和一种常见强碱,通常称为????????? 工业。
(5)加入“三种试剂”主要是为了除去粗食盐水中的Ca2+、Mg2+、SO42-等杂质,按加入的先后次序写出化学式??????????????????????????? 。
(6)制取“溶液B”的方法现在已作了改进,其原理图,用离子方程式表示该装置中发生的反应:????????????????????? 。

查看答案和解析>>
科目:高中化学 来源:0123 期中题 题型:不定项选择题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com