
 $\stackrel{Fe/HCl}{→}$
$\stackrel{Fe/HCl}{→}$ (苯胺,易被氧化);
(苯胺,易被氧化); ,最多有13个原子共面.
,最多有13个原子共面.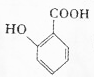 的名称为邻羟基苯甲酸,G中官能团名称为羧基、硝基.
的名称为邻羟基苯甲酸,G中官能团名称为羧基、硝基. .
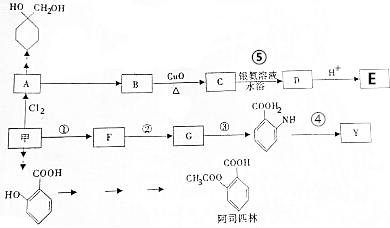
.分析 相对分子质量为92的某芳香烃甲,令分子组成为CxHy,则$\frac{92}{12}$=7…8,由烷烃中C原子与H原子关系可知,该烃中C原子数目不能小于7,故该芳香烃甲的分子式为C7H8,结构简式为 ,甲苯与氯气发生取代反应生成A,A转化生成B,B催化氧化生成C,C能与银氨溶液反应生成D,故B含有醇羟基、C含有醛基,故A为
,甲苯与氯气发生取代反应生成A,A转化生成B,B催化氧化生成C,C能与银氨溶液反应生成D,故B含有醇羟基、C含有醛基,故A为 ,B为
,B为 ,C为
,C为 ,D酸化生成E,故D为
,D酸化生成E,故D为 ,E为
,E为 ;
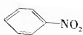
; 在浓硫酸、加热条件下与浓硝酸发生取代反应生成F,结合反应③的产物可知F为
在浓硫酸、加热条件下与浓硝酸发生取代反应生成F,结合反应③的产物可知F为 ,F转化生成G,由于苯胺容易被氧化,结合反应信息可知G为
,F转化生成G,由于苯胺容易被氧化,结合反应信息可知G为 .Y的结构中含有3个环状结构,是2分子
.Y的结构中含有3个环状结构,是2分子 形成2个肽键得到.
形成2个肽键得到.
解答 解:相对分子质量为92的某芳香烃甲,令分子组成为CxHy,则$\frac{92}{12}$=7…8,由烷烃中C原子与H原子关系可知,该烃中C原子数目不能小于7,故该芳香烃甲的分子式为C7H8,结构简式为 ,甲苯与氯气发生取代反应生成A,A转化生成B,B催化氧化生成C,C能与银氨溶液反应生成D,故B含有醇羟基、C含有醛基,故A为
,甲苯与氯气发生取代反应生成A,A转化生成B,B催化氧化生成C,C能与银氨溶液反应生成D,故B含有醇羟基、C含有醛基,故A为 ,B为
,B为 ,C为
,C为 ,D酸化生成E,故D为
,D酸化生成E,故D为 ,E为
,E为 ;
; 在浓硫酸、加热条件下与浓硝酸发生取代反应生成F,结合反应③的产物可知F为
在浓硫酸、加热条件下与浓硝酸发生取代反应生成F,结合反应③的产物可知F为 ,F转化生成G,由于苯胺容易被氧化,结合反应信息可知G为
,F转化生成G,由于苯胺容易被氧化,结合反应信息可知G为 .Y的结构中含有3个环状结构,是2分子
.Y的结构中含有3个环状结构,是2分子 形成2个肽键得到.
形成2个肽键得到.
(1)甲的结构简式为 ,旋转碳碳单键可以使甲基中1个H原子处于苯环平面内,最多有13个原子共面,
,旋转碳碳单键可以使甲基中1个H原子处于苯环平面内,最多有13个原子共面,
故答案为: ;13;
;13;
(2) 的名称为邻羟基苯甲酸,G为
的名称为邻羟基苯甲酸,G为 ,G中官能团名称为羧基、硝基,
,G中官能团名称为羧基、硝基,
故答案为:邻羟基苯甲酸;羧基、硝基;
(3)反应⑤是 与银氨溶液发生氧化反应生成
与银氨溶液发生氧化反应生成 ,反应方程式为:
,反应方程式为:
(4)反应①为取代反应,反应②为氧化反应,反应③为还原反应,反应④为取代反应,反应⑤为氧化反应,
故答案为:①④;
(5)阿司匹林同分异构体满足下列条件:①含有苯环;②既不能发生水解反应,也不能发生银镜反应,说明不含酯基和醛基;③1mol该有机物能与2molNaHCO3完全反应,说明含有两个羧基,
取代基为-CH(COOH)2,有1种结构;取代基为-COOH、-CH2COOH,有邻、间、对3种结构;取代基为两个-COOH、一个-CH3,两个-COOH处于邻位,-CH3有2种位置,两个-COOH处于间位,-CH3有23种位置,两个-COOH处于对位,-CH3有1种位置,符合条件的同分异构体共有10种,
故答案为:10.
点评 本题考查有机物的推断与合成,根据相对分子质量推断甲的结构是解题的关键,结合A的反应产物的结构特点、反应条件及反应信息利用正推法与逆推法相结合进行判断,是对有机物知识的综合考查,能较好的考查学生的阅读、分析与思维能力,是有机热点题型.


科目:高中化学 来源: 题型:选择题

| A. | M是阴离子交换膜 | B. | Y电极上产生无色气体 | ||
| C. | X电极区域可产生Mg(OH)2 | D. | X电极反应式为4OH--4e-═O2↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石油中含有1~50个碳原子的烷烃及环烷烃 | |
| B. | 石油分馏是物理变化,裂化、裂解和催化重整属于化学变化 | |
| C. | 石油裂化的目的主要是提高汽油的产量 | |
| D. | 裂化主要是将链烃变为芳香烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
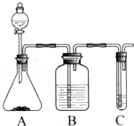 Ⅰ.实验室常用如图中的装置制备乙炔并检验乙炔的性质:
Ⅰ.实验室常用如图中的装置制备乙炔并检验乙炔的性质: ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
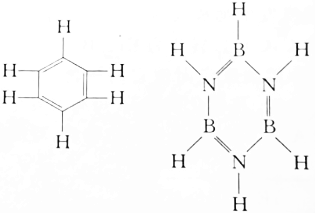
| A. | 前者大于后者 | B. | 前者等于后者 | C. | 前者小于后者 | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验序号 | 0.1032mol/L HCl溶液体积/mL | 待测NaOH溶液体积/mL |
| 1 | 27.83 | 25.00 |
| 2 | 26.53 | 25.00 |
| 3 | 27.85 | 25.00 |
| 化学式 | AgCl | AgBr | AgI | Ag2S | Ag2CrO4 |
| 颜色 | 白色 | 浅黄色 | 黄色 | 黑色 | 红色 |
| Ksp | 1.8×10-10 | 5.0×10-13 | 8.3×10-17 | 2.0×10-48 | 1.8×10-10 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
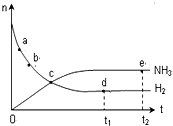 对于密闭容器中的反应:N2(g)+3H2(g)?2NH3(g),在673K、30MPa下,n(NH3)和n(H2)随时间的变化关系如下图所示,下列说法正确的是( )
对于密闭容器中的反应:N2(g)+3H2(g)?2NH3(g),在673K、30MPa下,n(NH3)和n(H2)随时间的变化关系如下图所示,下列说法正确的是( )| A. | 点a的正反应速率比点b的大 | |
| B. | 点c处反应达到平衡 | |
| C. | 点d (t1时刻)和点e (t2时刻)处n(N2)不一样 | |
| D. | 若开始充入1mol N2及足量H2,提供适当条件,可得2mol NH3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com