
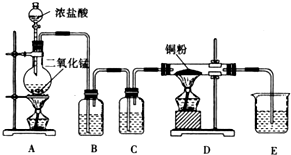
 某实验学习小组用MnO2和浓盐酸制取纯净干燥的氯气,并让氯气与铜粉反应制取纯净的无水CuCl2,装置如图所示.
某实验学习小组用MnO2和浓盐酸制取纯净干燥的氯气,并让氯气与铜粉反应制取纯净的无水CuCl2,装置如图所示.分析 (1)装置气密性检查的原理一般是通过压强差来产生明显的现象来判断;A中二氧化锰与浓盐酸在加热条件下反应生成氯气、氯化锰、水;
(2)浓盐酸易挥发,制备的氯气中含有氯化氢和水蒸气,依据氯气在饱和食盐水中溶解度不大,氯化氢易溶于水的性质选则饱和食盐水除去氯化氢,依据浓硫酸具有吸水性,选择浓硫酸除去水蒸气;
(3)铜在氯气中燃烧生成氯化铜;
(4)氯气有毒,直接排放到空气中能够引起空气污染,氯气能够与氢氧化钠反应,可以用氢氧化钠吸收过量的氯气;
(5)得到的无水CuCl2总是偏蓝色是因为E中水蒸气进入到D中,应在D、E之间增加一个含氯化钙的干燥管;
解答 解:(1)装置气密性检查的方法:装置连接好后,用手捂热圆底烧瓶,若B中有气泡产生,则气密性良好;
A中二氧化锰与浓盐酸在加热条件下反应生成氯气、氯化锰、水,化学方程式:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;故答案为:装置连接好后,用手捂热圆底烧瓶,若B中有气泡产生,则气密性良好;
MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;
(2)从A中制得的氯气含有杂质氯化氢、水蒸气,依次通过盛有饱和食盐水、和浓硫酸的洗气瓶除去;
故答案为:饱和食盐水;除去Cl2中的HCl;浓硫酸;除去Cl2中的水蒸气;
(3)铜在氯气中燃烧生成氯化铜,化学方法:Cu+Cl2 $\frac{\underline{\;点燃\;}}{\;}$ CuCl2;
故答案为:Cu+Cl2 $\frac{\underline{\;点燃\;}}{\;}$ CuCl2;
(4)氯气有毒,直接排放到空气中能够引起空气污染,氯气能够与氢氧化钠反应,可以用氢氧化钠吸收过量的氯气;
故答案为:吸收尾气Cl2 防止污染;
(5)得到的无水CuCl2总是偏蓝色是因为E中水蒸气进入到D中,应在D、E之间增加一个含氯化钙的干燥管;
故答案为:E中NaOH 中的水汽进入D中;在D、E之间增加一个含氯化钙的干燥管;
点评 本题考查了无水CuCl2的制备,设计氯气的实验室制备、净化和尾气处理,明确氯气制备原理和性质即可解答,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题

 .
. 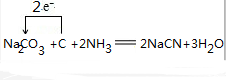 .
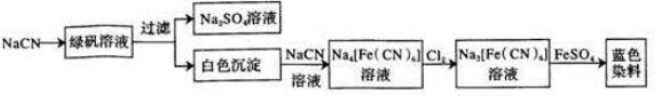
.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
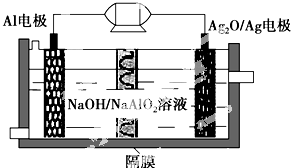 Al-Ag2O电池是一种可用作水下动力的优良电源,其原理如图所示.该电池工作时总反应式为2Al+3Ag2O+2NaOH═2NaAlO2+6Ag+H2O,则下列说法错误的是( )
Al-Ag2O电池是一种可用作水下动力的优良电源,其原理如图所示.该电池工作时总反应式为2Al+3Ag2O+2NaOH═2NaAlO2+6Ag+H2O,则下列说法错误的是( )| A. | 工作时正极发生还原反应 | |
| B. | 当电极上生成1.08 g Ag时,电路中转移的电子为0.01 mol | |
| C. | Al电极的反应式为Al-3e-+4OH-=AlO2-+2H2O | |
| D. | 工作时电解液中的Na+透过隔膜移向Al电极放电充电 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | 加入试剂 | 离子方程式 |
| NH4Cl(AlCl3)溶液 | ||
| NaHCO3(Na2CO3)溶液 | ||
| Fe 粉(Al粉) | ||
| FeCl3(FeCl2)溶液 |
 15.(18分)
15.(18分) ,反应类型是加聚反应.
,反应类型是加聚反应.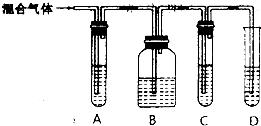
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用容量瓶前检查它是否漏水 | |
| B. | 容量瓶用蒸馏水洗净后,再用待配溶液润洗 | |
| C. | 盖好瓶塞,用食指顶住瓶塞,用另一只手指托住瓶底,把容量瓶倒转和摇动几次 | |
| D. | 容量瓶不能长期存放配制好的溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com