
分析 恰好完全反应,发生Fe+2FeCl3=3FeCl2,n(Fe)=$\frac{5.6g}{56g/mol}$=0.1mol,结合反应及c=$\frac{n}{V}$计算.
解答 解:n(Fe)=$\frac{5.6g}{56g/mol}$=0.1mol,发生Fe+2FeCl3=3FeCl2,可知n(FeCl3)=0.2mol,n(FeCl2)=0.3mol,则原FeCl3溶液的浓度为$\frac{0.2mol}{0.1L}$=2mol/L,反应后所得溶液的物质的量浓度为$\frac{0.3mol}{0.1L}$=3mol/L,
答:原FeCl3溶液及反应后所得溶液的物质的量浓度分别为2mol/L、3mol/L.
点评 本题考查化学反应的计算,为高频考点,把握发生的反应、物质的量关系为解答本题的关键,侧重分析与计算能力的考查,注意溶液体积不变,题目难度不大.


 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案科目:高中化学 来源: 题型:解答题
 甲醇可以与水蒸气反应生成氢气,反应方程式如下:
甲醇可以与水蒸气反应生成氢气,反应方程式如下:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{ab}{23}$mol | B. | $\frac{a(b+1)}{23}$mol | C. | $\frac{18ab}{23}$g | D. | $\frac{18a(b+1)}{23}$mol |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
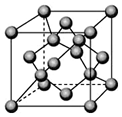 已知A、B、C、D都是元素周期表中前36号的元素.A元素的一种核素没有中子.B的基态原子核外电子有9种不同的运动状态;C元素是无机非金属材料的主角,它的单质可以用作电脑芯片;D元素是地壳中含量第二的金属元素.请回答:
已知A、B、C、D都是元素周期表中前36号的元素.A元素的一种核素没有中子.B的基态原子核外电子有9种不同的运动状态;C元素是无机非金属材料的主角,它的单质可以用作电脑芯片;D元素是地壳中含量第二的金属元素.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验 序号 | 实验内容 | 实验结果 |
| 1 | 加AgNO3溶液 | 有白色沉淀生成 |
| 2 | 加足量NaOH溶液并加热 | 收集到气体1.12L(已折算成标准状况下的体积) |
| 3 | 加足量BaCl2溶液时,对所得沉淀进行洗涤、干燥、称量;再向沉淀中加足量稀盐酸,然后干燥、称量 | 第一次称量读数为6.63g,第二次称量读数为4.66g |
| 阴离子符号 | 物质的量浓度(mol/L) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用二氧化钛作催化剂使水快速分解的同时放出大量热 | |
| B. | 该过程涉及到的反应为氧化还原反应 | |
| C. | 该反应的原理是:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2+O2 | |
| D. | 每产生氢气44.8L,转移电子数目为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 对二甲苯与酸性高锰酸钾溶液发生反应;甲烷与酸性高锰酸钾溶液不反应 | |
| B. | 甲苯与浓硝酸和浓硫酸混合液,加热;苯与浓硝酸和浓硫酸混合液,加热 | |
| C. | 乙苯与氢气在催化剂作用下加热反应;苯与氢气在催化剂作用下加热反应 | |
| D. | 邻二甲苯与氯气在光照下发生反应;甲烷在光照下与氯气发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
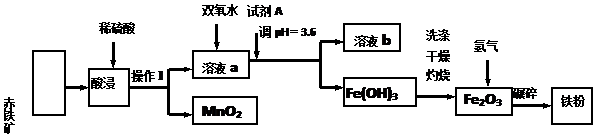
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe (OH)2 | Cu (OH)2 |
| pH | 3.4 | 5.2 | 9.7 | 6.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com