
下列有关元素及其化合物性质的比较正确的是( )
|
| A. | 原子半径:F<O<Al | B. | 稳定性:H2O<PH3<NH3 |
|
| C. | 酸性:H2CO3<H2SO4<H3PO4 | D. | 碱性:LiOH<NaOH<Al(OH)3 |
考点:
微粒半径大小的比较;金属在元素周期表中的位置及其性质递变的规律;非金属在元素周期表中的位置及其性质递变的规律.
专题:
元素周期律与元素周期表专题.
分析:
A.同周期自左而右原子半径减小,同主族自上而下原子半径逐渐增大;
B.非金属性越强,氢化物的稳定性越强;
C.非金属性越强,最高价氧化物对应水化物的酸性越强;
D.金属性越强,最高价氧化物对应水化物的碱性越强.
解答:
解:A.同周期自左而右原子半径减小,同主族自上而下原子半径逐渐增大,故原子半径F<O<Al,故A正确;
B.非金属性P<N<O,非金属性越强,氢化物的稳定性越强,则稳定性PH3<NH3<H2O,故B错误;
C.非金属性越强,最高价氧化物对应水化物的酸性越强,则酸性:H2CO3<H3PO4<H2SO4,故C错误;
D.金属性Al<Li<Na,金属性越强,最高价氧化物对应水化物的碱性越强,故碱性:Al(OH)3<LiOH<NaOH,故D错误,
故选A.
点评:
本题考查元素周期律的应用,注意掌握微粒半径比较规律、理解元素周期律,难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
下列关于丙烯(CH3﹣CH=CH2)的说法正确的( )
|
| A. | 丙烯分子有8个σ键,1个π键 |
|
| B. | 丙烯分子中3个碳原子都是sp3杂化 |
|
| C. | 丙烯分子不存在非极性键 |
|
| D. | 丙烯分子中3个碳原子在同一直线 |
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
|
| A. | 7.8 g苯中含有0.3NA个碳碳双键,0.3NA个碳碳单键 |
|
| B. | 5.6 g铁与足量的稀硝酸反应,失去电子数为0.2NA |
|
| C. | 32g硫(结构见图)含S﹣S的数目为NA
|
|
| D. | 含0.2 mol H2SO4的浓硫酸与足量铜反应,生成SO2的分子数为0.1 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
2008年9月,中国的三聚氰胺污染牛奶事件,在社会上造成了很坏的影响.牛奶和奶粉中添加三聚氰胺主要是因为它能冒充蛋白质.已知三聚氰胺中含有碳、氢、氮三种元素,为测定三聚氰胺的组成,用下列各仪器装置,在过量的氧气流中将2.52g三聚氰胺样品氧化成CO2、H2O和N2.请回答下列问题:
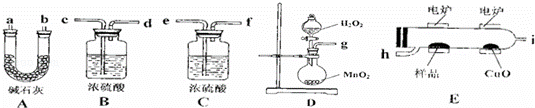
(1)产生的氧气按从左到右流向,所选择装置各导管的连接顺序是(要求:先用B、后用C):
g接 、 接 h、 接 、 、 接 .
(2)装置B的作用是 ;
装置E中CuO的作用是 ;
装置D中的化学方程式是 .
(3)实验前后称得A、C两装置的质量分别增加2.64g和1.08g,已知三聚氰胺的相对分子质量为126,则三聚氰胺的分子式为 .又知三聚氰胺分子中有3个氨基(﹣NH2),且有类似苯环的对称结构,试写出三聚氰胺的结构简式 .
(4)目前较多采用尿素为原料,在一定条件合成三聚氰胺.反应过程中,除生成CO2外,还生成一种使湿润的红色石蕊试纸变蓝的气体,试写出制备三聚氰胺的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,下列不发生反应的一组物质是( )
①铜与浓硫酸
②二氧化硅与NaOH溶液
③铜与浓硝酸
④石英与纯碱
⑤铁与液氯
⑥一氧化氮与氧气
⑦硅与氧气
⑧H2S与SO2.
|
| A. | ①②③⑥ | B. | ②③⑥⑧ | C. | ①④⑤⑦ | D. | ①②③⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:
如图为元素周期表中短周期的一部分,四种元素中只有一种是金属,下列说法错误的是( )
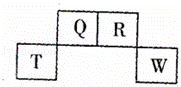
|
| A. | 气态氢化物稳定性:R>Q |
|
| B. | 元素T的离子结构示意图为 |
|
| C. | 与w同主族的某元素形成的18电子的氢化物分子中只有共价键没有离子键 |
|
| D. | Q可形成多种含氧酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
为测定镁铝合金(不含其它元素)中铝的质量分数,甲、乙、丙三个学习小组设计了下列三种不同的实验方案进行探究.请回答下列问题:
(一)甲组:实验方案:镁铝合金 测定剩余固体质量
测定剩余固体质量
实验步骤:
①称量:托盘天平称量一定质量镁铝合金粉末
②溶解:将①中药品加入烧杯中,加入过量的 NaOH 溶液,不断搅拌,充分反应.发生反应的离子方程式为: ↑
③过滤:
④洗涤:若未对过滤所得固体进行洗涤,测得铝的质量分数将 (填“偏高”、“偏低”或“不变”)
⑤干燥、称量剩余固体
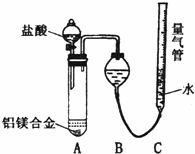
(二)乙组:实验方案:镁铝合金 测定生成气体的体积,实验装置如图所示.
测定生成气体的体积,实验装置如图所示.
(1)某同学提出该实验装置不够完善,应在A、B之间添加一个装有碱石灰的干燥装置.你的意见是
(填“需要”或“不需要”)
(2)为使测定结果尽可能精确,实验中应注意的问题是(要求写出二点): 、
(三)丙组:实验方案:12g镁铝合金 溶液
溶液
操作1包括过滤、洗涤、干燥和称量,并最终得到固体物质1.45g.则该合金中铝的质量分数为 95% .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应属于取代反应的是( )
|
| A. | C2H4+3O2 | B. | Zn+CuSO4═ZnSO4+Cu |
|
| C. | NaCl+AgNO3═AgCl↓+NaNO3 | D. | CH2Cl2+Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在100℃时,将0.100mol的N2O4气体充入1L抽空的密闭容器中,隔一定时间对该容器内的物质进行分析,得到如下表格:
| 时间/s 浓度mol•L﹣1 | 0 | 20 | 40 | 60 | 80 | 100 |
| c(N2O4)mol•L﹣1 | 0.100 | c1 | 0.050 | c3 | a | b |
| c(NO2)/mol•L﹣1 | 0.000 | 0.060 | c2 | 0.120 | 0.120 | 0.120 |
试填空:
(1)达到平衡时N2O4的转化率为 %.
(2)20s的四氧化二氮的浓度c1= mol•L﹣1,在0s~20s内四氧化二氮的平均反应速率为 mol•(L•s)﹣1;.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com