(2013?江苏三模)碳酸钠-过氧化氢加合物(aNa
2CO
3?bH
2O
2)具有漂白、杀菌作用.实验室用“醇析法”制备该物质的实验步骤如下:
第1步:取适量碳酸钠溶解于一定量水中,倒入烧瓶中;再加入少量稳定剂(MgCl
2和Na
2SiO
3),搅拌均匀.
第2步:将适量30%的H
2O
2溶液在搅拌状态下滴入烧瓶中,于15℃左右反应1h.
第3步:反应完毕后再加入适量无水乙醇,静置、结晶,过滤、干燥得产品.
(1)第1步中,稳定剂与水反应生成2种常见的难溶物,其化学方程式为
MgCl2+Na2SiO3+2H2O=2NaCl+Mg(OH)2↓+H2SiO3↓
MgCl2+Na2SiO3+2H2O=2NaCl+Mg(OH)2↓+H2SiO3↓
.
(2)第2步中,反应保持为15℃左右可采取的措施是
15℃水浴或冷水浴
15℃水浴或冷水浴
.
(3)第3步中,无水乙醇的作用是
降低碳酸钠-过氧化氢化合物的溶解度(有利于晶体析出)
降低碳酸钠-过氧化氢化合物的溶解度(有利于晶体析出)
.
(4)H
2O
2的含量可衡量产品的优劣.现称取m g(约0.5g)样品,用新煮沸过的蒸馏水配制成250mL溶液,取25.0mL于锥形瓶中,先用稀硫酸酸化,再用c mol?L
-1 KMnO
4溶液滴定至终点.
①配制250mL溶液所需的玻璃仪器有烧杯、玻璃棒、量筒、
(250mL)容量瓶
(250mL)容量瓶
、
胶头滴管
胶头滴管
.
②滴定终点观察到的现象是
溶液呈浅红色且30s内不褪色
溶液呈浅红色且30s内不褪色
.
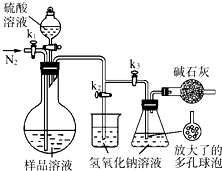
(5)可模拟用蒸馏法测定样品中碳酸钠的含量.装置如图所示(加热和固定装置已略去),实验步骤如下:
步骤1:按右图所示组装仪器,检查装置气密性.
步骤2:准确量取(4)中所配溶液50mL于烧瓶中.
步骤3:准确量取40.00mL约0.2mol?NaOH溶液2份,分别注入烧杯和锥形瓶中.
步骤4:打开活塞k
1、k
2,关闭活塞k
3,缓缓通入氮气一段时间后,关闭k
1、k
2,打开k
3;经滴液漏斗向烧瓶中加入10mL 3mol?硫酸溶液.
步骤5:加热至烧瓶中的液体沸腾,蒸馏,并保持一段时间.
步骤6:经k
1再缓缓通入氮气一段时间.
步骤7:向锥形瓶中加入酸碱指示剂,用c
1 mol?H
2SO
4标准溶液滴定至终点,消耗H
2SO
4标准溶液V
1 mL.
步骤8:将实验步骤1~7重复2次.
①步骤3中,准确移取40.00mL NaOH溶液所需要使用的仪器是
碱式滴定管
碱式滴定管
.
②步骤1~7中,确保生成的二氧化碳被氢氧化钠溶液完全吸收的实验步骤是
1,5,6
1,5,6
(填序号).
③为获得样品中碳酸钠的含量,还需补充的实验是
用H2SO4标准溶液标定NaOH溶液的浓度
用H2SO4标准溶液标定NaOH溶液的浓度
.



 阅读快车系列答案
阅读快车系列答案

 (2013?江苏三模)碳酸钠-过氧化氢加合物(aNa2CO3?bH2O2)具有漂白、杀菌作用.实验室用“醇析法”制备该物质的实验步骤如下:
(2013?江苏三模)碳酸钠-过氧化氢加合物(aNa2CO3?bH2O2)具有漂白、杀菌作用.实验室用“醇析法”制备该物质的实验步骤如下: