
| 熔点/℃ | 沸点/℃ | 水溶性 |
| -59.5 | 11.0 | 极易溶解 |
| A. | 化学方程式中的a=l,b=2 | |
| B. | 草酸起到还原剂的作用 | |
| C. | KC1O3中只有Cl元素被还原 | |
| D. | 在标准状况下生成5.6L C1O2,转移0.2mol电子 |
分析 A、根据C、H原子守恒计算;
B、反应中H2C2O4中碳元素的化合价由+3价升高到+4价,则为还原剂;
C、反应中KC1O3中Cl元素由+5价降低为+4价,则为氧化剂被还原;
D、根据Cl元素的化合价变化来分析电子转移的数目.
解答 解:A、2KC1O3+aH2C2O4+H2SO4=2C1O2↑+K2SO4+2CO2↑+bH2O,根据C、H原子守恒,则a=l,b=2,故A正确;
B、反应中H2C2O4中碳元素的化合价由+3价升高到+4价,则H2C2O4为还原剂,起到还原剂的作用,故B正确;
C、反应中KC1O3中Cl元素由+5价降低为+4价,则Cl元素被还原,故C正确;
D、反应中Cl元素由+5价降低为+4价,则在标准状况下生成5.6 LC1O2,转移0.25 mol电子,故D错误;
故选D.
点评 本题考查氧化还原反应,明确元素的化合价变化即可解答,难度不大,注意草酸中碳元素的化合价计算利用氢为+1价、氧为-2价及化合价原则来解答.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,22.4LH2O中含有分子数为NA | |
| B. | 常温常压下,28gCO和N2的混合物所含的质子数为14NA | |
| C. | 1molCl2分别与足量的铁或氢氧化钠溶液反应,转移电子数均为2NA | |
| D. | 常温下,1mol/L Na2CO3溶液中阴离子总数等于NA |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. |  长时间看到Fe(OH)2白色沉淀 | B. | 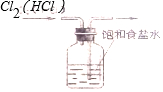 除去Cl2中的HCl杂质 | ||
| C. | 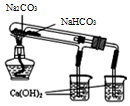 比较NaHCO3、Na2CO3的热稳定性 | D. | 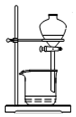 分离碘酒中的碘和酒精 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6种 | B. | 7种 | C. | 8种 | D. | 9种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCl和NaOH反应的中和热△H=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ/mol | |
| B. | CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)=2CO(g)+O2(g)反应的△H=+566.0kJ/mol | |
| C. | 铁粉与硫粉需要加热才能发生的反应,则此反应是吸热反应 | |
| D. | 1mol甲烷燃烧生成水和二氧化碳所放出的热量就是甲烷燃烧热 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
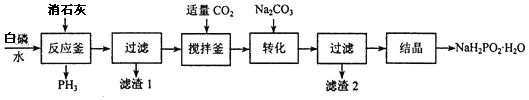
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分别取两种固体样品,加热产生气体的是碳酸氢钠 | |
| B. | 分别取样溶于水后加入氯化钙溶液,若有白色沉淀则是碳酸钠 | |
| C. | 分别取样溶于水后加入澄清石灰水,若有白色沉淀则是碳酸钠 | |
| D. | 分别取等质量的两种固体样品,与足量的硫酸反应,产生气体较多的是碳酸氢钠 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com