
| A、含氢元素的化合物中一定有氢键 |
B、因为分子间存在氢键的缘故,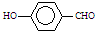 比 比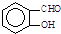 熔沸点高 熔沸点高 |
| C、由于氢键比范德华力强,所以H2O分子比H2S分子稳定 |
| D、“可燃冰”--甲烷水合物(例如:8CH4?46H2O)中CH4与H2O之间存在氢键 |
 中两个基团靠得很近,与
中两个基团靠得很近,与 相比,不容易形成分子间氢键;
相比,不容易形成分子间氢键; 中两个基团靠得很近,不容易形成分子间氢键;而
中两个基团靠得很近,不容易形成分子间氢键;而 的两个基团靠得较远,容易形成分子间氢键,故
的两个基团靠得较远,容易形成分子间氢键,故 比
比 的熔沸点高,故B正确;
的熔沸点高,故B正确;

科目:高中化学 来源: 题型:
| A、铁与盐酸的反应:2Fe+6H+=2Fe3++3H2↑ |
| B、石灰石与稀盐酸反应制备二氧化碳:CO32-+2H+=H2O+CO2↑ |
| C、向氢氧化铜中滴加硫酸溶液:H++OH-=H2O |
| D、硫酸铜溶液和氢氧化钡溶液混合:Cu2++SO42-+Ba2++2OH-=Cu(OH)2↓+BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 26g |
| 100g |
| A、△H-T△S<0△S<0 |
| B、△H-T△S<0△S>0 |
| C、△H-T△S>0△S>0 |
| D、△H-T△S>0△S<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CO2和SO2中物质的量比为 1:1 |
| B、CO2和SO2的密度比为1:1 |
| C、CO2和SO2的物质的量浓度比为11:16 |
| D、CO2和SO2中所含氧原子个数比为1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、蒸发、蒸馏、萃取 |
| B、萃取、蒸馏、蒸发 |
| C、蒸发、萃取、蒸馏 |
| D、蒸馏、萃取、蒸发 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com