
| A. | 3molH2+1molN2 | B. | 2molNH3+1molN2 | ||
| C. | 2molN2+3molH2 | D. | 0.1molNH3+0.95molN2+2.85molH2 |
分析 反应2NH3?3H2+N2,在恒温恒容下,达到平衡时,容器内N2的百分含量也为a%,说明与原平衡是等效平衡,按化学计量数转化到方程式的左边,满足n(NH3)=2mol即可,据此进行分析.
解答 解:根据等效平衡,按化学计量数转化到方程式的左边,满足n(NH3)=2mol,则达到平衡时,容器内N2的百分含量为a%,
A.3molH2+1molN2按化学计量数转化到方程式的左边可得:n(NH3)=2mol,属于等效平衡,故A正确;
B.2molNH3+1molN2与初始量2molNH3不相同,则不属于等效平衡,达到平衡时,容器内N2的百分含量不是a%,故B错误;
C.2molN2+3molH2按化学计量数转化到方程式的左边,不满足n(NH3)=2mol,与初始初始加入物质不同,不是等效平衡,故C错误;
D.0.1molNH3+0.95molN2+2.85molH2,按化学计量数转化到方程式的左边,满足n(NH3)=2mol,属于等效平衡,故D正确;
故选AD.
点评 本题考查化学平衡的有关计算,题目难度中等,正确构建平衡建立的途径是解题关键,注意掌握等效平衡的含义及应用方法,试题培养了学生的分析能力及灵活应用能力.


 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案科目:高中化学 来源: 题型:实验题
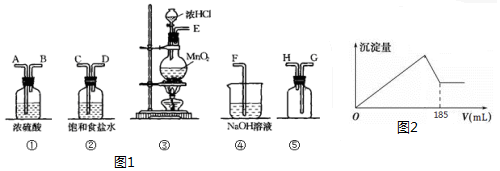
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金刚石燃烧比石墨燃烧放出的热量少 | |
| B. | 等质量是石墨燃烧放热多 | |
| C. | 石墨的能量比金刚石的能量高 | |
| D. | 由石墨制备金刚石一定是吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
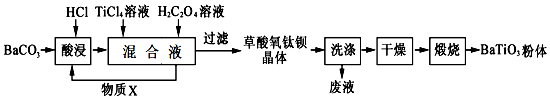
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 13g锌与一定量浓硫酸恰好完全反应,生成气体的分子数为0.2NA | |
| B. | 71g氯气通入足量的水中,反应中转移的电子总数为NA | |
| C. | 由D和18O所组成的水11g,所含的中子数为4NA | |
| D. | 1molBrCl与H2O完全反应生成氯化氢和次溴酸,转移的电子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl-、Br-、CO32- | B. | Br-、CO32-、Cl- | C. | CO32-、Br-、Cl- | D. | Br-、Cl-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
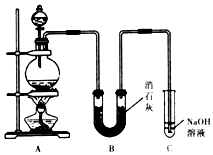 某学生设计如图所示的实验装置,利用氯气与潮湿的消石灰反应制取漂白粉,据此回答下列问题:
某学生设计如图所示的实验装置,利用氯气与潮湿的消石灰反应制取漂白粉,据此回答下列问题: MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O CaCl2+Ca(ClO)2+2H2O
CaCl2+Ca(ClO)2+2H2O查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com