
【题目】下列关于新制氯水及久置氯水的说法中不正确的是( )
A.新制的氯水呈黄绿色,久置的氯水变为无色
B.新制的氯水漂白作用强,久置的氯水漂白作用很弱
C.新制的氯水所含微粒种类多,久置的氯水所含微粒种类较少
D.新制的氯水中无氯离子,久置的氯水中含有氯离子
【答案】D
【解析】
A. 新制氯水中含有氯气,呈黄绿色,而久置氯水溶质为HCl,溶液为无色,故A正确;
B. 新制氯水含有次氯酸,具有漂白性,HClO不稳定,见光易分解,久置氯水中HClO浓度较小,漂白作用很弱,故B正确;
C. 氯气与水发生Cl2+H2O![]() HCl+HClO,水也发生电离,所以新制氯水含有Cl2、HClO、H+、Cl-、ClO-、OH-等粒子,HClO不稳定,见光易分解,促进平衡向正反应方向移动,久置的氯水可看作是浓度很稀的盐酸,只含有H+、Cl-、OH-等粒子,故C正确;
HCl+HClO,水也发生电离,所以新制氯水含有Cl2、HClO、H+、Cl-、ClO-、OH-等粒子,HClO不稳定,见光易分解,促进平衡向正反应方向移动,久置的氯水可看作是浓度很稀的盐酸,只含有H+、Cl-、OH-等粒子,故C正确;
D.氯气与水发生Cl2+H2O![]() HCl+HClO,新制氯水含有Cl2、HClO、H+、Cl-、ClO-、OH-等粒子,故D错误;
HCl+HClO,新制氯水含有Cl2、HClO、H+、Cl-、ClO-、OH-等粒子,故D错误;
故选D。


科目:高中化学 来源: 题型:
【题目】用示意图或图示的方法能够直观形象地将化学知识传授给学生,下列示意图或图示正确的是( )
A.砷原子的结构示意图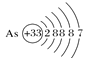 B.BF4—的结构式
B.BF4—的结构式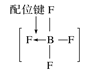
C.HF分子间的氢键 D.丙氨酸的手性异构
D.丙氨酸的手性异构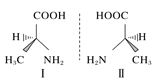
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒容密闭容器中通入X并发生反应:2X(g) ![]() Y(g),T1、T2温度下X的物质的量浓度c(X)随时间t变化的曲线如图所示,下列叙述正确的是( )
Y(g),T1、T2温度下X的物质的量浓度c(X)随时间t变化的曲线如图所示,下列叙述正确的是( )
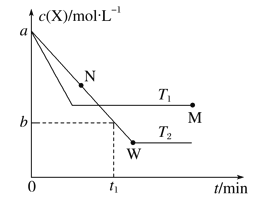
A. 该反应进行到M点放出的热量大于进行到W点放出的热量
B. T2温度下,在0~t1时间内,v(Y)=![]() mol·L-1·min-1
mol·L-1·min-1
C. M点的正反应速率v正大于N点的逆反应速率v逆
D. M点时再加入一定量Y,平衡后X体积分数与原平衡相比增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是部分短周期元素的常见化合价与原子序数的关系:
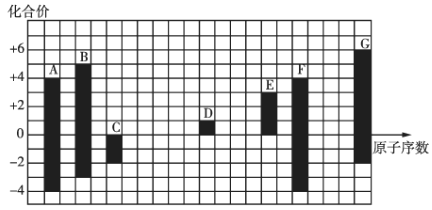
(1)元素![]() 在元素周期表中的位置是__________________。
在元素周期表中的位置是__________________。
(2)其中金属性最强的元素是______(用元素符号表示,下同),非金属性最强的元素是______。
(3)![]() 、
、![]() 、
、![]() 的半径由大到小的顺序是__________(用离子符号表示)。
的半径由大到小的顺序是__________(用离子符号表示)。
(4)最简单氢化物的稳定性:![]() ______
______![]() (填“
(填“![]() ”或“
”或“![]() ”)。
”)。
(5)![]() 、
、![]() 、
、![]() 元素最高价氧化物对应水化物的酸性:_____(用化学式表示,下同)
元素最高价氧化物对应水化物的酸性:_____(用化学式表示,下同)![]() ______
______![]() ______。
______。
(6)![]() 与
与![]() 形成的具有强氧化性的化合物为______(填化学式),该化合物与
形成的具有强氧化性的化合物为______(填化学式),该化合物与![]() 反应的化学方程式为________________________,其中氧化剂与还原剂的物质的量之比为____________。
反应的化学方程式为________________________,其中氧化剂与还原剂的物质的量之比为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关系图中,A是一种正盐,B是气态氢化物,C是单质,F是强酸。当X无论是强酸还是强碱时都有如下转化关系(其他反应产物及反应所需条件均已略去),当X是强碱时,过量的B跟Cl2反应除生成C外,另一产物是盐酸盐。
![]()
下列说法中不正确的是( )
A. 当X是强酸时,A、B、C、D、E、F中均含同一种元素,F可能是H2SO4
B. 当X是强碱时,A、B、C、D、E、F中均含同一种元素,F是HNO3
C. B和Cl2的反应是氧化还原反应
D. 当X是强酸时,C在常温下是气态单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在150℃时使NH4HCO3分解,将所产生的气体依次通过Na2O2和浓H2SO4,则Na2O2增重ag,浓H2SO4增重bg;若将上述气体先通过浓H2SO4,则使酸液增重dg,再通过Na2O2,则使之增重cg。设气体皆完全被吸收,a、b、c、d质量由大到小的排列顺序正确的是
A.d a c bB.b c a dC.a c b dD.d c b a
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废旧钴金属片中的钴有+2价和+3价,还含有锰、铁、钙、镁、铝等金属元素及碳粉等,回收钴的工艺流程如下:
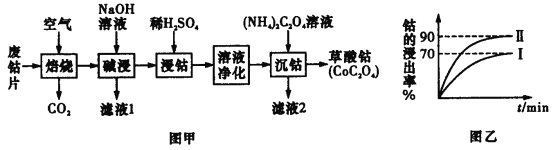
(1)焙烧时为了使废旧钴金属片充分反应,可采取的措施是____________________(任写一条)。
(2)该流程中浸钴时,钴的浸出率最高只能达到70%,后来改进方法,加入使用硫酸进行第一次浸取后,再加入Na2SO3溶液进行第二次浸取,从而使钴的浸出率达90%以上,写出第二次浸出钴时溶液中发生反应的离子方程式:____________________。
(3)净化溶液的操作中含有多个步骤,先除铁后除锰。
①除铁:常温下,调节溶液pH为1.5~2.0后,加H2O2,反应一段时间,加8%Na2CO3溶液,将溶液的pH调至4.0~5.0。已知Fe(OH)3的溶度积常数为4×10-38,则当溶液的pH调至4.0时,溶液中的c(Fe3+)=__________mol·L-1。
②除锰:加入NaClO溶液。写出该离子方程式:____________________。
③减钙镁:加入NH4F溶液,沉淀大部分的钙、镁的离子。

试解释为何草酸铵溶液沉钴前要减钙镁:______________________________。
(4)滤液2的主要成分为____________________(以化学式表示)。
(5)得到的草酸钴沉淀须洗涤干燥。写出检验沉淀已被洗净的操作与现象__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】500mLKNO3和Cu(NO3)2的混合溶液中c(NO3-)=6.0mol·L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4L气体(标准状况),假定电解后溶液体积仍为500mL,下列说法正确的是( )
A.原混合溶液中c(K+)为2mol·L-1
B.上述电解过程中共转移4 mol电子
C.电解得到的Cu的物质的量为0.5mol
D.电解后溶液中c(H+)为2mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,属于同分异构体的是( )
A.![]() 和
和![]()
B.H2N-CH2-COOH 和 H3C-CH2-NO2
C.CH3-CH2-CH2-COOH 和 H3C-CH2-CH2-CH2-COOH
D.H3C-CH2-O-CH2-CH3 和![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com