
 C(g)+D(g)��Ӧ��ƽ�ⳣ�����¶ȵĹ�ϵ���£�
C(g)+D(g)��Ӧ��ƽ�ⳣ�����¶ȵĹ�ϵ���£�| |�¶�/ �� | 700 | 900 | 830 | 1000 | 1200 |
| ƽ�ⳣ�� | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
 A(g)+B(g)��ƽ�ⳣ����ֵΪ ��
A(g)+B(g)��ƽ�ⳣ����ֵΪ ��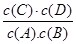 ��1�֣� <��1�֣�
��1�֣� <��1�֣�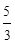 ��1�֣�
��1�֣�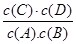 ���¶����ߣ�ƽ�ⳣ����С������Ӧ������У�Ϊ���ȷ�Ӧ������ӦΪ���ȷ�Ӧ����H<0��
���¶����ߣ�ƽ�ⳣ����С������Ӧ������У�Ϊ���ȷ�Ӧ������ӦΪ���ȷ�Ӧ����H<0��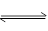 C(g)+D(g)��Ӧ��ƽ�ⳣ���ĵ�������1/0.6=
C(g)+D(g)��Ӧ��ƽ�ⳣ���ĵ�������1/0.6=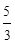 ��
��

 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 Fe(s)+ CO2(g) ��H>0
Fe(s)+ CO2(g) ��H>0�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 3C(g)�����������У���˵����Ӧ�Ѵﵽƽ�����
3C(g)�����������У���˵����Ӧ�Ѵﵽƽ������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
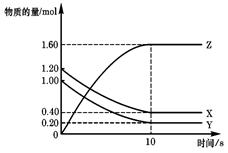
| A��ƽ��ʱX��Y��ת������ͬ |
| B���ﵽƽ��������������Ϊ4 L��ƽ�������ƶ� |
| C��ƽ��ʱX������Ӧ������Y���淴Ӧ������� |
D��T��ʱ���÷�Ӧ�Ļ�ѧ����ʽΪ��X (g)+Y(g)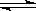 2Z(g)��ƽ�ⳣ��K="40" 2Z(g)��ƽ�ⳣ��K="40" |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
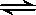 2C(g)���ﵽƽ��ʱ�������ʵ����ʵ���֮��Ϊn(A)��n(B)��n(C)=2��2��1�������¶Ȳ��䣬��2��2��1�����ʵ���֮���ٳ���A��B��C��������˵����ȷ����
2C(g)���ﵽƽ��ʱ�������ʵ����ʵ���֮��Ϊn(A)��n(B)��n(C)=2��2��1�������¶Ȳ��䣬��2��2��1�����ʵ���֮���ٳ���A��B��C��������˵����ȷ���� �鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 H2(g)��I2(g) ��H<0����t1ʱ�ﵽƽ�⣬t2ʱ�������²����£���t3ʱ�ִﵽ��ƽ�⣬������һ�仯��ͼ����
H2(g)��I2(g) ��H<0����t1ʱ�ﵽƽ�⣬t2ʱ�������²����£���t3ʱ�ִﵽ��ƽ�⣬������һ�仯��ͼ���� 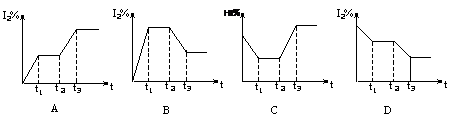
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2SO3(g)�ǹ�ҵ���������Ҫ��Ӧ֮һ��һ���¶��£��ڼס��ҡ��������ݻ���Ϊ2L�ĺ����ܱ�������Ͷ��SO2(g)��O2(g)������ʼ���ʵ�����SO2��ƽ��ת�������±���ʾ��
2SO3(g)�ǹ�ҵ���������Ҫ��Ӧ֮һ��һ���¶��£��ڼס��ҡ��������ݻ���Ϊ2L�ĺ����ܱ�������Ͷ��SO2(g)��O2(g)������ʼ���ʵ�����SO2��ƽ��ת�������±���ʾ��| | �� | �� | �� | |
| ��ʼ���ʵ��� | n(SO2) / mol | 0.4 | 0.8 | 0.8 |
| n(O2) / mol | 0.24 | 0.24 | 0.48 | |
| SO2��ƽ��ת���� / % | 80 | ��1 | ��2 | |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 B(g)��C(g)��������A����ʼŨ��Ϊ1.0 mol��L-1������B��C����ʼŨ��Ϊ0ʱ������A��Ũ�ȡ�ת�����Լ�����B��Ũ���淴Ӧʱ��ı仯�����и�ͼ��ʾ��
B(g)��C(g)��������A����ʼŨ��Ϊ1.0 mol��L-1������B��C����ʼŨ��Ϊ0ʱ������A��Ũ�ȡ�ת�����Լ�����B��Ũ���淴Ӧʱ��ı仯�����и�ͼ��ʾ��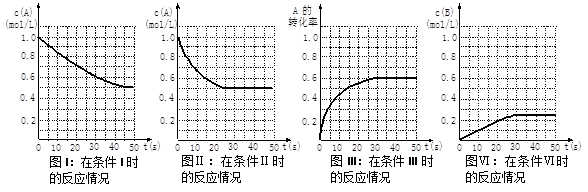
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 H����A�����ش��������⣺
H����A�����ش��������⣺�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com