
| A.反应物总能量为679kJ |
| B.生成物总能量为431kJ |
| C.氢气和氯气反应生成2 mol氯化氢气体,反应放出183 kJ·mol-1能量 |
| D.氢气和氯气反应生成2 mol氯化氢气体,反应吸收183 kJ·mol-1能量 |
 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案科目:高中化学 来源:不详 题型:单选题
| A.等物质的量的硫蒸气和固体硫分别完全燃烧,前者放出热量多 |
| B.1mol碳和2mol碳的燃烧热不相同 |
| C.在101kPa时,2g氢气完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)= 2H2O(l)△H=-285.8kJ/mol |
| D.在稀溶液中,H+ (aq) + OH- (aq) = H2O (l)△H=-57.3kJ/mol,若将0.5 mol 浓硫酸与1mol 氢氧化钠溶液混合,放出的热量大于57.3kJ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.C+H2O=CO+H2 ΔH =" +10.9" kJ/ mol |
| B.C(s)+H2O(g)=CO(g)+H2(g) ΔH =" +10.94" kJ/ mol |
| C.C(s)+H2O(g)=CO(g)+H2(g) ΔH =" +131.28" kJ/ mol |
| D.1/2C(s)+ 1/2H2O(g)=" 1/2CO(g)+" 1/2H2(g ) ΔH =" +" 65.64 kJ/ mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.S(s)+O2(g)= SO2(g);△H=-269.8kJ/mol |
| B.中和热的热化学方程式:NaOH(aq)+HCl(aq)= NaCl(aq)+H2O(l);△H=+57.3kJ/mol |
| C.燃烧热的热化学方程式: C2H5OH(l)+3O2(g)= 2CO2(g)+3H2O(g);△H=-1367.0 kJ/mol |
| D.2NO2 = O2+2NO;△H = +116.2kJ/mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.CO+H2O=CO2+H2;△H="+41" kJ/mol |
| B.CO(g)+H2O(g)=CO2(g)+H2(g);;△H= ?41 kJ/mol |
| C.CO2(g)+H2(g)=CO(g)+H2O(g);△H="+41" kJ/mol |
| D.CO2(g)+H2(g) =CO(g)+H2O(g);△H=?41 kJ/mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.一定大于92.0 kJ | B.一定等于92.0 kJ | C.一定小于92.0 kJ | D.不能确定 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH1=-99 kJ·mol-1
2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH1=-99 kJ·mol-1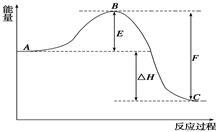
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com