
����Ŀ����ͼ��ʾ3��ʵ��װ�ã��ֱ�ش��������⣺ 
��1��װ��1Ϊ����������ʴʵ�飮һ��ʱ��������̼���IJ���Ͳ�ڵ����̪��Һ���ɹ۲쵽̼����������Һ��죬�õ缫��ӦΪ ��
��2��װ��2�е�ʯī���������������������װ�÷������ܷ�Ӧ�����ӷ���ʽΪ ��
��3��װ��3�м��ձ�ʢ��100mL 0.2molL��1��NaCl��Һ�����ձ�ʢ��100mL 0.5molL��1��CuSO4��Һ����Ӧһ��ʱ���ֹͣͨ�磮ȡ��Cu�缫��ϴ�ӡ�����������缫���� 0.64g��
�ٵ�Դ��M��Ϊ�������ձ������缫�ĵ缫��ӦΪ��
�����ձ��е�ⷴӦ�����ӷ���ʽΪ��
�ۼס������ձ������ɵ������״���¹�mL��
���𰸡�
��1��O2+4e��+2H2O�T4OH��
��2������2Fe3++Cu�T2Fe2++Cu2+
��3������Fe��2e���TFe2+��2Cu2++2H2O ![]() 2Cu+O2��+4H+��224
2Cu+O2��+4H+��224
���������⣺��1��װ��1Ϊ����������ʴʵ�飬�����绯ѧ��ʴ����Ϊ������̼Ϊ�������۲쵽̼����������Һ��죬˵����̼���������õ�������OH�����ӣ���Ӧ�ĵ缫��ӦʽΪO2+4e��+2H2O�T4OH�� �� ���Դ��ǣ�O2+4e��+2H2O�T4OH������2��װ��2Ϊԭ��أ�����ΪCu���缫��ӦΪ��Cu��2e���TCu2+ �� ����Ϊʯī���缫��ӦΪ2Fe+2e���T2Fe2+ �� ��Ӧ���ܷ���ʽΪ2Fe3++Cu�T2Fe2++Cu2+ �� ���Դ��ǣ�����2Fe3++Cu�T2Fe2++Cu2+����3���ٷ�Ӧһ��ʱ���ֹͣͨ�磮����ձ��е��뼸�η�̪���۲쵽ʯī�缫�������ȱ�죬˵����ʯī�缫������OH�����ӣ��缫��ӦΪ��2H2O+2e���T2OH��+H2����������ԭ��Ӧ��Ϊ���ص����������ӵ�Դ�ĸ�������M��Ϊ������N��Ϊ������������ӦΪFe��2e���TFe2+ �� ���Դ��ǣ�����Fe��2e���TFe2+�������ձ��������ͭ��Һ��ʯīΪ�������缫��ӦΪ4OH����4e���TO2��+H2O��CuΪ�����缫��ӦΪCu2++2e���TCu�������ܷ�ӦΪ2Cu2++2H2O ![]() 2Cu+O2��+4H+ ��
2Cu+O2��+4H+ ��
���Դ��ǣ�2Cu2++2H2O ![]() 2Cu+O2��+4H+����ȡ��Cu�缫��ϴ�ӡ�����������缫����0.64g��������Cu�����ʵ���Ϊ
2Cu+O2��+4H+����ȡ��Cu�缫��ϴ�ӡ�����������缫����0.64g��������Cu�����ʵ���Ϊ ![]() =0.01mol��ת�Ƶĵ��ӵ����ʵ���Ϊ0.01mol��2=0.02mol��
=0.01mol��ת�Ƶĵ��ӵ����ʵ���Ϊ0.01mol��2=0.02mol��
���ݼ��ձ���������ĵ缫��Ӧ������������������
2H2O+ | 2e�� | �T | 2OH��+ | H2�� |
2mol | 22.4L | |||
0.02mol | V |
V= ![]() =0.224L����224ml�����Դ��ǣ�224��
=0.224L����224ml�����Դ��ǣ�224��


 �ƸԺ���ȫ�����Ų��Ծ�ϵ�д�
�ƸԺ���ȫ�����Ų��Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ʢ�й���ϡ������Թ��У���Ӱ�������������ʵ������ǣ� ��
A.�����Ũ��
B.�����ı����
C.��Һ���¶�
D.������Na2SO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������������ЧӦ�ķ�ɢϵ��
A. ˮ B. ʯ��ˮ C. �� D. ������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڼ��顢��ϩ�������Ҵ��������У���ȷ����
A.��������ˮB.���ܷ����ӳɷ�Ӧ
C.���ܷ���������ӦD.���ǻ�ʯȼ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£���2L���ܱ������У�X��Y��Z������������ʵ�����ʱ��仯��������ͼ��ʾ������������ȷ���ǣ� ��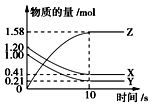
A.��Ӧ��ʼ��10 s����Z��ʾ�ķ�Ӧ����Ϊ0.079mol��Ls����1
B.��Ӧ��ʼ��10 s��X�����ʵ���Ũ�ȼ�����0.79molL��1
C.�÷�Ӧ���ǿ��淴Ӧ
D.��Ӧ�Ļ�ѧ����ʽΪX��g��+Y��g��Z��g��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й������ʵ���Ũ�ȱ�����ȷ���ǣ�������
A.0.2mol/LNa2SO4��Һ�к���Na+��SO42�������ʵ���Ϊ0.6mol
B.��1Lˮ����22.4L�Ȼ��⣨����£����������Ũ����1mol/L
C.10g 98%�����ᣨ�ܶ�Ϊ1.84gcm��3����10mL 18.4mol/L�������Ũ����ͬ
D.50mL 2mol/LNaCl��Һ��100 mL 0.5mol/LMgCl2��Һ�У�Cl�����ʵ���Ũ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ�ҿ�����һ������ﮩ�����أ��������ܶȼ��ߣ�Ч�ʴ�90%���ϣ���������ӵ⻯ﮣ�LiI������ˮ������ԭ����ͼ��ʾ���ܷ�ӦΪ��O2+4LiI+2H2O ![]() 2I2+4LiOH
2I2+4LiOH
���ڸõ�ص�����˵������ȷ���ǣ� ��
A.�ŵ�ʱ������I�� ������
B.���ʱLi+������������������
C.���ʱ������ӦΪLiOH+e���TLi+OH��
D.�ŵ�ʱ������ӦΪO2+2H2O+4Li++4e���T4LiOH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ѡ���У���Ԫ�����ڱ��ڲ����������Ա仯����
A. ԭ�Ӱ뾶B. ���ϼ�
C. ԭ������D. Ԫ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��V mL Al2(SO4)3��Һ�к�Al3��a g��ȡ ![]() mL��Һϡ�͵�4 V mL����ϡ�ͺ���Һ��SO
mL��Һϡ�͵�4 V mL����ϡ�ͺ���Һ��SO ![]() �����ʵ���Ũ����( )
�����ʵ���Ũ����( )
A.![]() mol��L��1
mol��L��1
B.![]() mol��L��1
mol��L��1
C.![]() mol��L��1
mol��L��1
D.![]() mol��L
mol��L
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com