
某地污水中含有Zn2+、Hg2+、Fe3+、Cu2+四种阳离子。甲、乙、丙三位同学设计的从该污水中回收金属铜的方案如下:
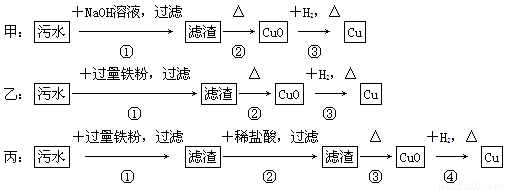
下列判断正确的是( )。
A.三种实验方案都能制得纯净的铜
B.乙方案中加过量铁粉可以将四种阳离子全部还原
C.甲方案中的反应涉及置换、分解、化合、复分解四种反应类型
D.丙方案会产生环境污染
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案科目:高中化学 来源:2014高考名师推荐化学--线索综合5 题型:简答题
A~G各物质间的关系如下图,其中B、D为气态单质.
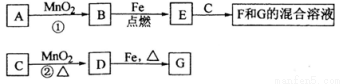
请回答下列问题:
(1)物质C和E的名称分别为________、________;
(2)可选用不同的A进行反应①若能在常温下进行,其化学方程式为________;
若只能在加热情况下进行,则反应物A应为________;
(3)反应②的化学方程式为_____________________;
(4)新配制的F溶液应加入________以防止其转化为G,检验G溶液中阳离子的常用试剂是________,实验现象为________________。
查看答案和解析>>
科目:高中化学 来源:2014江苏常熟市高二化学期末模拟4(必修2、选修4、结构)试卷(解析版) 题型:实验题
(10分)某研究小组为了研究不同条件下金属铝粉在过量稀硫酸中的溶解性能,设计如下实验。已知:c(H2SO4)=4.5 mol·L-1,反应均需要搅拌60min。
编号 | 温度/℃ | 加入某盐 | H2SO4体积/mL | H2O体积/mL | 铝粉加入量/g | 铝粉溶解量 /g |
① | 20 | 不加 | 40 | 0 | 2.0050 | 0.0307 |
② | 80 | 不加 | 40 | 0 | 2.0050 | 0.1184 |
③ | t1 | 不加 | 20 | V1 | 2.0050 | ﹨ |
④ | t2 | 5 mL0.01 mol·L-1 CuSO4溶液 | 20 | V2 | 2.0050 | ﹨ |
(1)实验①和②的目的是 。
为了获得铝粉溶解量,还需要测量的数据是 。
(2)实验①和③是为了研究硫酸的浓度对该反应的影响,则t1= ℃,V1= mL。
(3)实验③和④是为了研究加入CuSO4溶液对该反应的影响,则t2= ℃,V2= mL。
研究表明,在相同条件下加入少量CuSO4有利于Al的溶解。原因是 。
查看答案和解析>>
科目:高中化学 来源:2014江苏常熟市高二化学期末模拟4(必修2、选修4、结构)试卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.使苯酚显紫色的溶液:NH4+、K+、SCN-、NO3-
B.0.1mol·L-1HNO3溶液: Na+、Mg2+、SO42-、Cl-
C.0.5mol·L-1FeCl3溶液:K+、Na+、I-、SO42-
D.由水电离产生的c(H+)=10-13 mol·L-1的溶液:K+、Na+、Cl-、HCO3-
查看答案和解析>>
科目:高中化学 来源:2014年高考化学鲁科版4.3铜及其化合物 金属材料与复合材料练习卷(解析版) 题型:填空题
四氯化钛(TiCl4)是制取航天航空工业材料——钛合金的重要原料。由钛铁矿(主要成分是FeTiO3)制备TiCl4等产品的一种工艺流程示意如下:
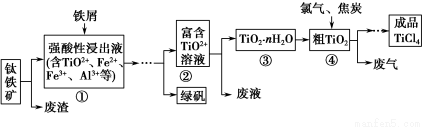
回答下列问题:
(1)往①中加入铁屑至浸出液显紫色,此时溶液仍呈强酸性。该过程中有如下反应发生:
2Fe3++Fe=3Fe2+
2TiO2+(无色)+Fe+4H+=2Ti3+(紫色)+Fe2++2H2O
Ti3+(紫色)+Fe3++H2O=TiO2+(无色)+Fe2++2H+
加入铁屑的作用是 。
(2)在②→③工艺过程中需要控制条件以形成TiO2·nH2O溶胶,该溶胶的分散质颗粒直径大小在 范围。
(3)若把③中制得的固体TiO2·nH2O用酸清洗除去其中的Fe(OH)3杂质,还可制得钛白粉。已知25 ℃时,Ksp[Fe(OH)3]=2.79×10-39,该温度下反应Fe(OH)3+3H+??Fe3++3H2O的平衡常数K= 。
(4)已知:TiO2(s)+2Cl2(g)=TiCl4(l)+O2(g) ΔH=+140 kJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH=-221 kJ·mol-1
写出④中TiO2和焦炭、氯气反应生成液态TiCl4和CO气体的热化学方程式: 。
(5)上述工艺具有成本低、可用低品位矿物为原料等优点。依据绿色化学理念,该工艺流程中存在的不足之处是 (只要求写出一项)。
(6)依据下表信息,要精制含少量SiCl4杂质的TiCl4,可采用 方法。
| TiCl4 | SiCl4 |
熔点/℃ | -25.0 | -68.8 |
沸点/℃ | 136.4 | 57.6 |
查看答案和解析>>
科目:高中化学 来源:2014年高考化学鲁科版4.3铜及其化合物 金属材料与复合材料练习卷(解析版) 题型:选择题
日本地震后,导致福岛第一核电站引发核危机。核反应堆的第一层护罩是锆锡合金外壳,第二层护罩是压力仓,第三层护罩是用最坚固的钢和混凝土制成的非常厚的球体。下列叙述错误的是( )。
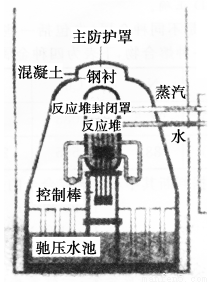
A.锆锡合金、钢、混凝土都属于混合物
B.钢的硬度和熔沸点都高于纯铁
C.锆锡合金和钢属于金属材料,混凝土属于传统的硅酸盐材料
D.在高温下,钢和水蒸气可发生反应产生氢气
查看答案和解析>>
科目:高中化学 来源:2014年高考化学鲁科版4.1硅 无机非金属材料练习卷(解析版) 题型:选择题
寿山石主要成分为叶蜡石,叶蜡石组成为Al2O3·4SiO2·H2O,下列观点不正确的是( )。
A.寿山石雕刻作品要避免与酸、碱接触
B.寿山石颜色丰富多彩是因为含有不同形态的金属氧化物
C.潮湿的空气可能导致寿山石作品表面溶解变质
D.置于干燥空气中可能会导致寿山石作品脱水变质
查看答案和解析>>
科目:高中化学 来源:2014年高考化学鲁科版2.5铁及其化合物练习卷(解析版) 题型:选择题
下列各图示中能较长时间看到Fe(OH)2白色沉淀的是( )。

A.①②③④⑤ B.①②③⑤
C.①②③④ D.②③④⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com