

 ).B与HCl发生加成反应生成C,则C为CH3CH2Cl,C与氨气发生取代反应生成F.F与丙发生反应生成普鲁卡因,由普鲁卡因的结构可知,丙为
).B与HCl发生加成反应生成C,则C为CH3CH2Cl,C与氨气发生取代反应生成F.F与丙发生反应生成普鲁卡因,由普鲁卡因的结构可知,丙为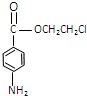 ,
,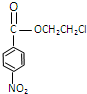 发生还原反应是生成丙,E与乙反应生成
发生还原反应是生成丙,E与乙反应生成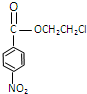 ,可推知乙为
,可推知乙为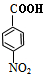 ,则甲苯发生硝化反应生成甲为
,则甲苯发生硝化反应生成甲为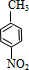 ,甲发生氧化反应生成乙,据此解答.
,甲发生氧化反应生成乙,据此解答. ).B与HCl发生加成反应生成C,则C为CH3CH2Cl,C与氨气发生取代反应生成F.F与丙发生反应生成普鲁卡因,由普鲁卡因的结构可知,丙为
).B与HCl发生加成反应生成C,则C为CH3CH2Cl,C与氨气发生取代反应生成F.F与丙发生反应生成普鲁卡因,由普鲁卡因的结构可知,丙为 ,
,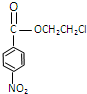 发生还原反应是生成丙,E与乙反应生成
发生还原反应是生成丙,E与乙反应生成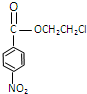 ,可推知乙为
,可推知乙为 ,则甲苯发生硝化反应生成甲为
,则甲苯发生硝化反应生成甲为 ,甲发生氧化反应生成乙,
,甲发生氧化反应生成乙, ,故答案为:
,故答案为: ;
; ,
, ;
;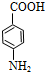 ,
, 的同分异构体符合:a.分子结构中含苯环,且每个苯环有2个侧链,b.分子结构中一定含官能团-NH2,且-NH2直接与碳原子相连,侧链为-NH2、-COOH,有邻、间、对三种(包含
的同分异构体符合:a.分子结构中含苯环,且每个苯环有2个侧链,b.分子结构中一定含官能团-NH2,且-NH2直接与碳原子相连,侧链为-NH2、-COOH,有邻、间、对三种(包含 ),侧链为-NH2、-OOCH,有邻、间、对三种,侧链为-CH2NH2、-OH,有邻、间、对三种,故符合条件的同分异构体共有9种,故答案为:9.
),侧链为-NH2、-OOCH,有邻、间、对三种,侧链为-CH2NH2、-OH,有邻、间、对三种,故符合条件的同分异构体共有9种,故答案为:9.


 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、自然界“水滴石穿”的主要原因用方程式表示为:CaCO3+H2O+CO2═Ca(HCO3)2 |
| B、“雨后彩虹”是与胶体、光学等知识有关的自然现象 |
| C、人类目前直接利用的能量大部分是由化学反应产生的 |
| D、“生物固氮”是指植物通过叶片直接吸收空气中的氮气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||

| 实验方案 | 预期现象 | |
| a | 加NaOH溶液 | 产生白色沉淀,变灰绿再变红褐 |
| b | 先加KSCN溶液,再加氯水 | 先无明显现象,后变红 |
| c | 加酸性KMnO4溶液 | 紫色褪去 |
| d | 先加氯水,再加KSCN溶液 | 溶液先变黄,再变红 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ① | ② | |||||
| ③ | ④ | ⑤ | ⑥ | ⑦ |

查看答案和解析>>
科目:高中化学 来源: 题型:
 某化学兴趣小组将两份等质量的硫粉分别在空气、氧气中燃烧,放出的热量是一样多还是不一样多?经过讨论、综合,根据观点分成了两组.
某化学兴趣小组将两份等质量的硫粉分别在空气、氧气中燃烧,放出的热量是一样多还是不一样多?经过讨论、综合,根据观点分成了两组.查看答案和解析>>
科目:高中化学 来源: 题型:

| Ph | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
| 钒沉淀率/ | 88 | 92 | 93 | 95 | 95 | 95 | 93 | 90 | 87 |
查看答案和解析>>
科目:高中化学 来源: 题型:
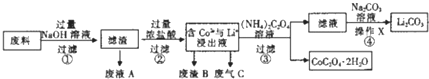
| 编号 | 温度/℃ | 时间/min | 盐酸浓度/mol?L-1 | 钴浸出率/% |
| 1 | 80 | 120 | 3.04 | 97.82 |
| 2 | 80 | 150 | 3.04 | 100.0 |
| 3 | 80 | 180 | 3.04 | 100.0 |
| 4 | 80 | 150 | 2.28 | 100.0 |
| 5 | 80 | 150 | 1.52 | 80.26 |
| 6 | 70 | 150 | 2.28 | 86.85 |
| 7 | 90 | 150 | 2.28 | 100.0 |
| 8 | 80 | 150 | 2.28 | 100.6 |
| 温度/℃ | 0 | 30 | 60 | 90 |
| 浓度/mol?L-1 | 0.21 | 0.17 | 0.14 | 0.10 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com