
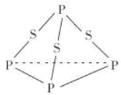
【题目】三硫化磷(P4S3)是黄绿色针状晶体,易燃、有毒,分子结构之一如图所示。下列有关P4S3的说法中不正确的是( )
A.P4S3中各原子最外层均满足 8 电子稳定结构
B.P4S3中磷元素为+ 3 价
C.P4S3中 P 原子和 S 原子均为 sp3杂化
D.1molP4S3分子中含有 6mol 极性共价键
【答案】B
【解析】
A. 磷原子最外层电子数为5,硫原子最外层电子数为6,从图中可看出,P4S3中每个磷原子形成了3个共价键,每个硫原子形成了2个共价键,所以P4S3分子中所有原子均满足8电子稳定结构,A正确;
B. P4S3分子中,有一个磷原子连接了3个硫原子,其化合价为+3,其他的磷原子都是连接两个磷原子和一个硫原子,其化合价为+1,B错误;
C.从图中可看出该分子中,每个磷原子形成3个σ键且有一对孤电子对,每个硫原子形成2个σ键且有两对孤电子,所以,该分子中硫原子和磷原子均采取杂sp3化,C正确;
D.一个P4S3分子中含有6个P—S键和3个P—P键,P—S键属于极性键,P—P键属于非极性键,所以1mol P4S3中含有6mol极性键,D正确;
故答案为:B。


科目:高中化学 来源: 题型:
【题目】如图是部分短周期元素的单质及其化合物(或其溶液)的转化关系。已知在常温常压下,A是固体,B、C、D、E是非金属单质且都是气体,C呈黄绿色;化合物F是淡黄色固体,化合物G的焰色反应为黄色,化合物Ⅰ和J通常状况下呈气态;D和E反应生成一种刺激性气味的气体。
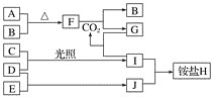
请回答下列问题:
(1)E和J的化学式分别是________和________。
(2)写出F和CO2反应的化学方程式并用单线桥法表示电子转移的情况:_________。
(3)将少量单质C通入盛有淀粉碘化钾溶液的试管中,溶液变蓝色,该反应的离子方程式为_________。
(4)标况下3.36 L气体B与A完全反应,转移电子的数目为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年新发现的元素鉝(Lv)是116号主族元素,其原子核外最外层电子数是6。下列说法不正确的是 ( )
A.Lv位于第七周期第VIA族B.Lv在同主族元素中金属性最弱
C.Lv的同位素原子具有相同的电子数D.中子数为177的Lv核素符号为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,W、X、Y、Z为短周期主族元素,Y和Z两元素的原子序数之和等于W元素的原子序数。下列说法错误的是( )
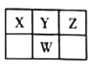
A.X、Y、W分别与Z都能形成两种或两种以上的化合物,这些化合物都能与NaOH反应
B.X、Y、Z都能形成10、18 电子的氢化物分子,其中X的最简单氢化物沸点最低
C.Y、Z、W与氢四种元素能组成离子化合物,该化合物能发生水解
D.最高价氧化物对应水化物的酸性:Y>W>X
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】球墨铸铁中含有一种铁碳化合物X。实验室测定化合物X的组成实验如下:下列说法不正确的是

A. 固体2是氧化铁
B. X与足量的热浓硝酸反应可能有NO2和CO2生成
C. 溶液甲中可能含有Fe3+
D. X的化学式可以表示为Fe3C2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
碱金属及碳族元素在科研领域、生活和生产方面有广泛的应用。回答下列问题:
(1)在元素周期表中,与Li的化学性质最相似的邻族元素是__________(填元素符号),该元素基态原子最外层电子的自旋状态___________(填“相同”或“相反”)。
(2)碳和硅的有关化学键键能如下所示:
化学键 | C-H | C-O | Si-H | Si-O |
键能/kJmol-1 | 413 | 336 | 318 | 452 |
SiH4的稳定性小于CH4,更易生成氧化物,原因是__________________。
(3)天然硅酸盐都是由[SiO4]四面体以顶角氧原子相连而成,可成链状也可成环,所以硅酸盐种类繁多。下图a代表SiO44-,b、c是硅氧四面体形成的环状结构。
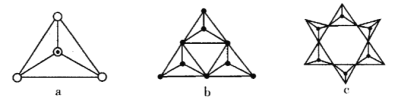
硅氧四面体中Si的轨道杂化类型为____________; 图b环状结构硅酸根的化学式为______________若在环状结构中硅的原子数为n,写出环状结构中硅酸根的通式_____________。
(4)钾与溴作用能形成溴化钾晶体,该晶体类型为___________,其晶格能可通过下图的Borm-Haber循环计算得到。

从上图可知,K原子的第一电离能为_____ kJ/mol, Br-Br键键能为______kJ/ mol,KBr的晶格能为______kJ/mol,晶格能越大,该晶体的熔点越______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关叙述及相关解释均正确的是( )
选项 | 叙述 | 解释 |
A | 键的极性的强弱:N-H>O-H>F-H | 电负性:N<O<F |
B | 石墨的熔点高于金刚石 | 碳碳键的键长:石墨<金刚石 |
C | 熔点: | Ⅰ形成分子内氢键,Ⅱ形成分子间氢键 |
D | 酸性:HI>HBr>HCl | HI、HBr、HCl中的范德华力逐渐减小 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】产自我国西北某盐湖的“块碱”是一种Na2CO3和NaCl的混合物。可通过以下方法对块碱样品的组成和含量进行分析测定。
I.定性测定NaCl的存在:
(1)取样品少许溶于水,加入足量稀硝酸充分反应后再滴加______溶液,能观察到有______________产生,说明块碱中含有NaCl。
II.定量测定Na2CO3的含量:准确称量w g样品置于如图所示的装置中,向其中加入足量稀硫酸,通过测定生成气体的体积来求算Na2CO3的含量。请回答下列相关问题:
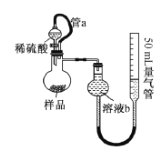
(2)测定装置中,导管a的作用是__________________。
(3)为提高测定的准确度,溶液b最宜选用__________________。
①饱和食盐水 ②饱和NaHCO3溶液 ③澄清石灰水 ④酸性KMnO4溶液
(4)以下是测量收集到气体体积必须包括的几个步骤:①调整橡胶管所连两装置液面高度使之相同;②使装置内的气体都冷却至室温;③读取碱式滴定管的示数。这三步操作的正确顺序是:________(请填写步骤代号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图所示装置进行以下实验,能得到相应实验结论的是
① | ② | ③ | 实验结论 |
| |
A | 浓氨水 | NaOH | 酚酞 | NaOH的碱性比 NH3H2O的强 | |
B | 浓盐酸 | MnO2 | 淀粉溶液 | 非金属性:氯元素大于碘元素 | |
C | 浓硝酸 | Na2CO3 | Na2SiO3 | 酸性:HNO3 > H2CO3 > H2SiO3 | |
D | 浓硫酸 | 蔗糖 | 溴水 | 浓硫酸具有脱水性、氧化性 |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com