
| A. | 在25℃时,次氯酸的电离方程式及热效应可表示为:HClO(aq)=H+(aq)+ClO-(aq)△H=-(57.3+Q1)kJ•mol-1 | |
| B. | 将20mL 1mol/L HClO与10mL1mol/L NaOH混合后的溶液,一定存在:2c(H+)-2c(OH-)=c(ClO-)-c(HClO) | |
| C. | 将0.2mol/L NaClO 与0.1mol/L HCl等体积混合后的溶液,溶液显碱性,则存在:c(ClO-)>c(Cl-)>c(HClO)>c(OH-) | |
| D. | 已知酸性CH3COOH>HClO,则等浓度CH3COONa和NaClO的混合液中:c(Na+)>c(ClO-)>c(CH3COO-)>c(OH-)>c(H+) |
分析 A.根据盖斯定律书写次氯酸的电离及热效应方程式;
B.二者完全反应后,溶液中溶质为等物质的量浓度的HClO和NaClO,任何电解质溶液中都存在质子守恒;
C.二者完全反应后,溶液中溶质为等物质的量浓度的NaClO、HClO和NaCl,溶液呈碱性,说明HClO的电离程度小于NaClO水解程度;
D.酸性CH3COOH>HClO,则酸根离子水解程度ClO->CH3COO-,酸根离子水解程度越大则该酸根离子在水溶液中浓度越小,这两种酸根离子都水解导致溶液呈碱性.
解答 解:A.根据盖斯定律①-②得HClO(aq)=H+(aq)+ClO-(aq)△H=-(Q1-57.3)kJ•mol-1,故A错误;
B.二者完全反应后,溶液中溶质为等物质的量浓度的HClO和NaClO,任何电解质溶液中都存在质子守恒得2c(H+)+c(HClO)=c(ClO-)+2c(OH-),所以得2c(H+)-2c(OH-)=c(ClO-)-c(HClO),故B正确;
C.二者完全反应后,溶液中溶质为等物质的量浓度的NaClO、HClO和NaCl,溶液呈碱性,说明HClO的电离程度小于NaClO水解程度,则微粒浓度大小顺序是c(HClO)>c(Cl-)>c(ClO-)>c(OH-),故C错误;
D.酸性CH3COOH>HClO,则酸根离子水解程度ClO->CH3COO-,酸根离子水解程度越大则该酸根离子在水溶液中浓度越小,这两种酸根离子都水解导致溶液呈碱性,离子浓度大小顺序是c(Na+)>c(CH3COO-)>c(ClO-)>c(OH-)>c(H+),故D错误;
故选B.
点评 本题考查离子浓度大小比较,为高频考点,明确溶液中溶质成分及其性质、水解程度或电离程度大小是解本题关键,注意守恒思想的应用,题目难度不大.


 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:选择题
| A. | 该混盐的水溶液呈碱性 | |
| B. | 该混盐溶液中加人BaCl2溶液,可以生成白色沉淀 | |
| C. | 该混盐与稀硫酸反应产生1mol S时转移2NA个电子 | |
| D. | 该混盐中的硫元素的化合价为-2和+4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验 | 现象 | 结论 |
| A | 将浓硫酸入蔗糖中 | 固体变黑后发生膨胀 | 浓硫酸具有吸水性和强还原性 |
| B | 将两小粒相同的钠分别投入乙醇和水中 | 钠在水中反应比在乙醇中剧烈 | 相同条件下,水的电离能力比乙醇强 |
| C | 向某溶液滴加氯水后再滴入KCSN溶液 | 溶液变为红色 | 该溶液中一定含有Fe2+ |
| D | 常温时将铝片加入浓硝酸中 | 未出现气泡 | 常温下铝与浓硝酸不反应 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加水 | B. | CH3COONa固体 | C. | 升温 | D. | NaCl固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
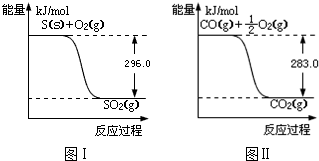
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (注:R、R′为径基).A为有机合成中间体,可发生银镜反应.A在一定条件下发生消去反应,可能得到两种互为同分异构体的产物,其中的一种B可用于制取合成树脂、染料等多种化工产品.A能发生如图所示的变化.
(注:R、R′为径基).A为有机合成中间体,可发生银镜反应.A在一定条件下发生消去反应,可能得到两种互为同分异构体的产物,其中的一种B可用于制取合成树脂、染料等多种化工产品.A能发生如图所示的变化.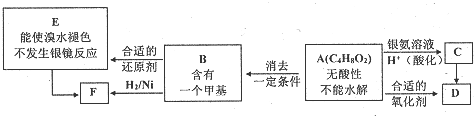
 或
或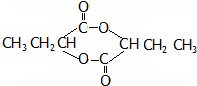 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | K1、K2闭合时,Na+均移向铁棒 | |
| B. | K1闭合,石墨棒周围溶液pH逐渐升高 | |
| C. | K2闭合,铁棒不会被腐蚀,属于牺牲阳极的阴极保护法 | |
| D. | K2闭合,电路中通过0.4NA个电子时,两极共产生标况下4.48L气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 非金属元素的两原子之间不可能形成离子键 | |
| B. | 离子化合物不可能全部由非金属元素组成 | |
| C. | 含有非极性键的分子不一定是共价化合物 | |
| D. | 离子化合物中一定含有离子键. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
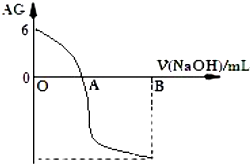
| A. | A 点时加入氢氧化钠溶液体积为 20 mL | |
| B. | OA 段溶液中:c(CH3COO-)>c(CH3COOH) | |
| C. | 室温时 0.01 mol/L的醋酸溶液 pH=4 | |
| D. | 若 B 点时加入 NaOH 溶液为 40 mL,所得溶液中:c(CH3COO-)+c(CH3COOH)=c(OH-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com